
【2025年度版】肺がん治療全解説!治療や新薬、喫煙との関係とは?
【YouTube動画でご覧になりたい方はこちら】
 濱元誠栄院長
濱元誠栄院長こんにちは、銀座みやこクリニック院長の濱元です。
今回は肺がん治療完全ガイド2025というテーマでお話させていただきます(2024年11月1日現在の情報です)。
肺がんのり患患者数と死亡者数
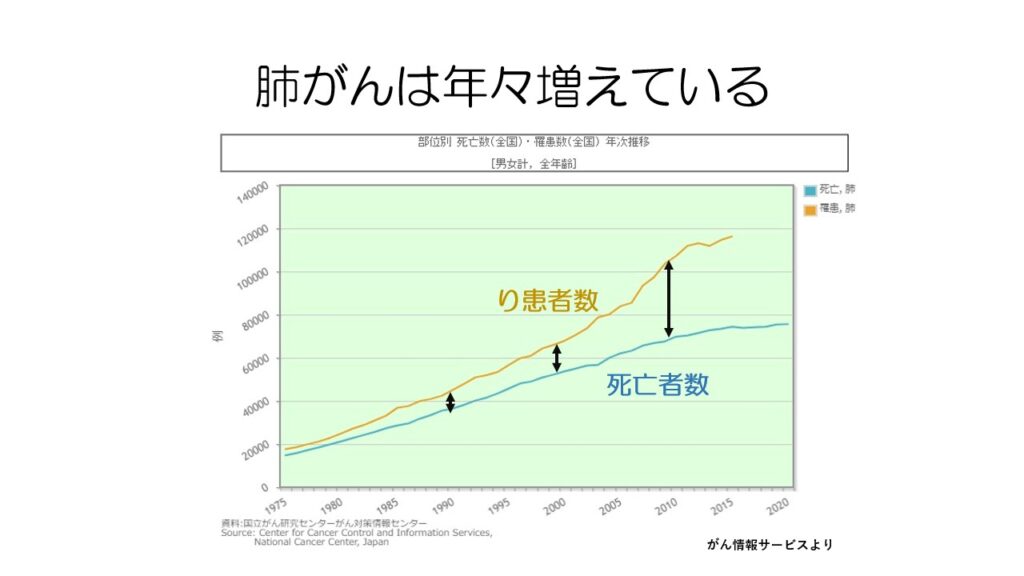
肺がんは罹患者数も死亡者数も年々増え続けています。
ただ、昔と比べて罹患者数の増加に対する死亡者数の割合がが減ってきています。
これはつまり、昔より肺がんが治る病気になってきたということです。
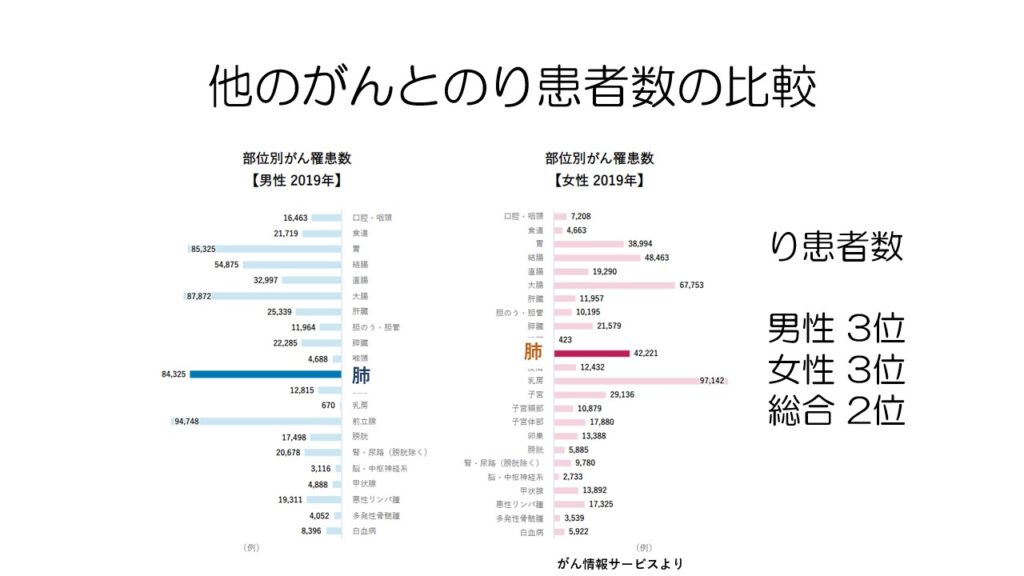
肺がんは、全がん患者の中で男性で3位、女性で3位、男女合わせると2位となっています。

他のがんと死亡者数を比較してみると、肺がんは男性で1位、女性で2位、男女合わせると1位となっており、がんの中で最も死亡者数が多いがんです。
昔より治るようになってきたものの、まだまだ治療が難しいがんと言えます。
肺がんの原因

肺がんの最も多い原因はタバコです。
その他、アスベストやヒ素などの有害物質、PM2.5などの大気汚染も原因となります。
最近では、女性ホルモンとの関連も示唆されています。
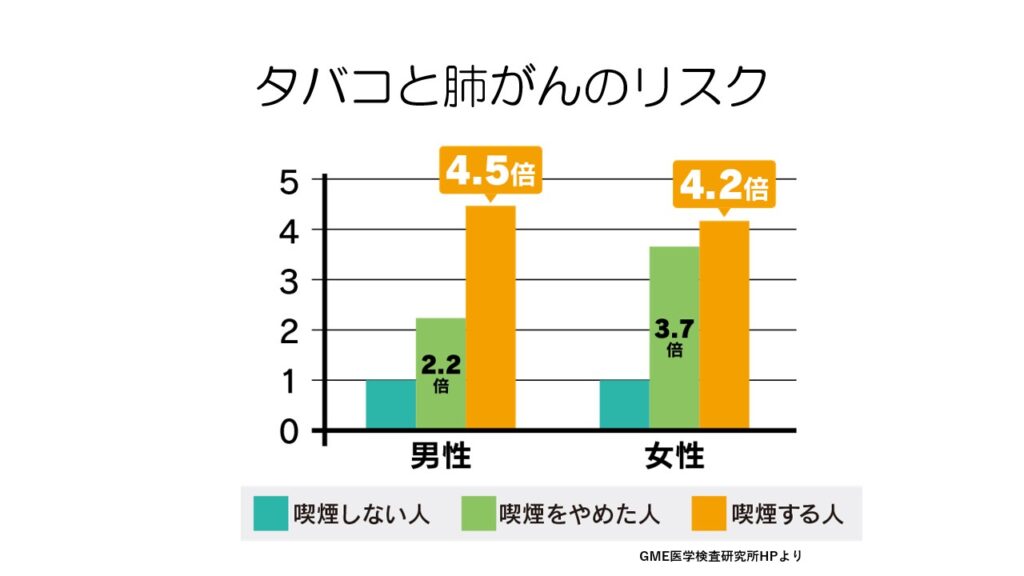
喫煙者は、非喫煙者と比較してリスクが4倍以上に上がります。
禁煙をした人でもリスクは高いので、喫煙しないのが一番の予防です。
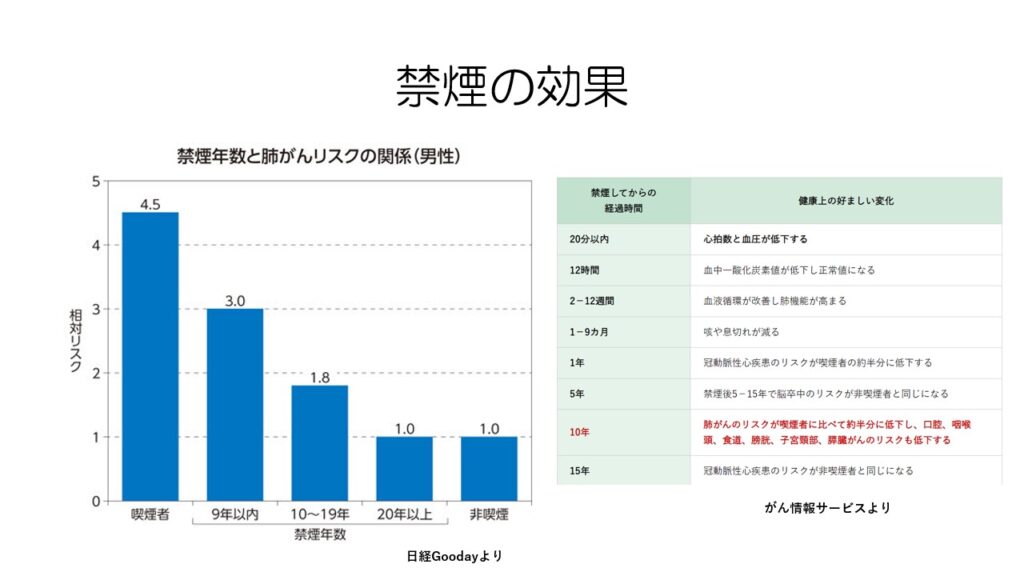
禁煙をしてもしばらくは肺がんのリスクは残りますが、禁煙年数が長くなるにつれてリスクは下がっていきます。
20年以上禁煙した場合、非喫煙者と同程度のリスクまで低下します。
女性はもう少し早くリスクが低下すると言われています。
他にも禁煙すると様々な効果が見られます。

喫煙者が減っているのに肺がんが増えているので、肺がんとタバコは関係ないという説を唱える人がいます。
年齢調整死亡率で見てみると、1995年を境に肺がんの死亡率は低下してきています。
喫煙を始めてから肺がんになるまでに数十年のタイムラグがあるため、喫煙者が減少した効果が遅れて現れてきています。
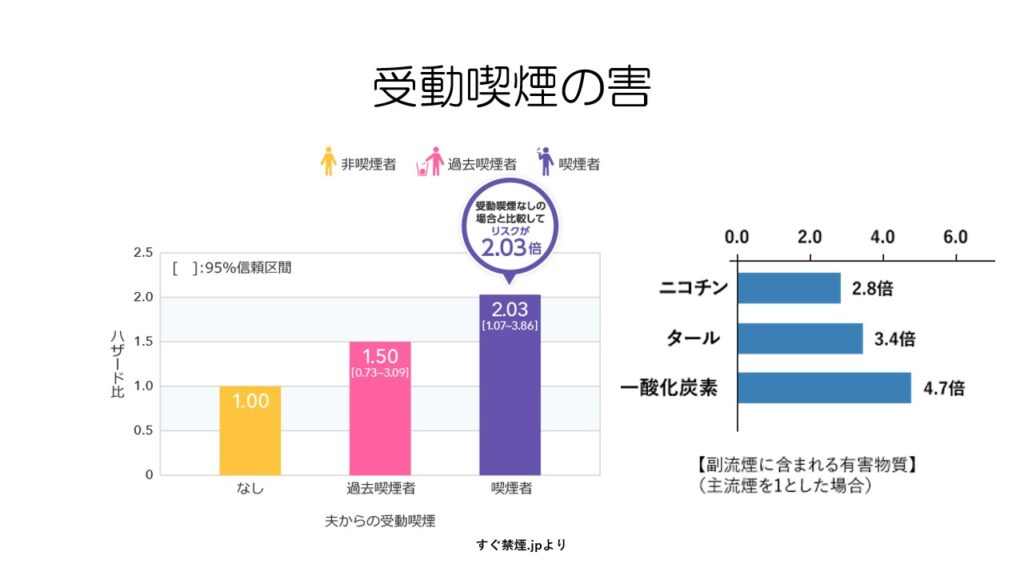
旦那さんからの受動喫煙で配偶者の肺がんリスクが2倍に上昇します。
また、副流煙に含まれる有害物質は喫煙者の主流煙よりも数倍多く含まれています。
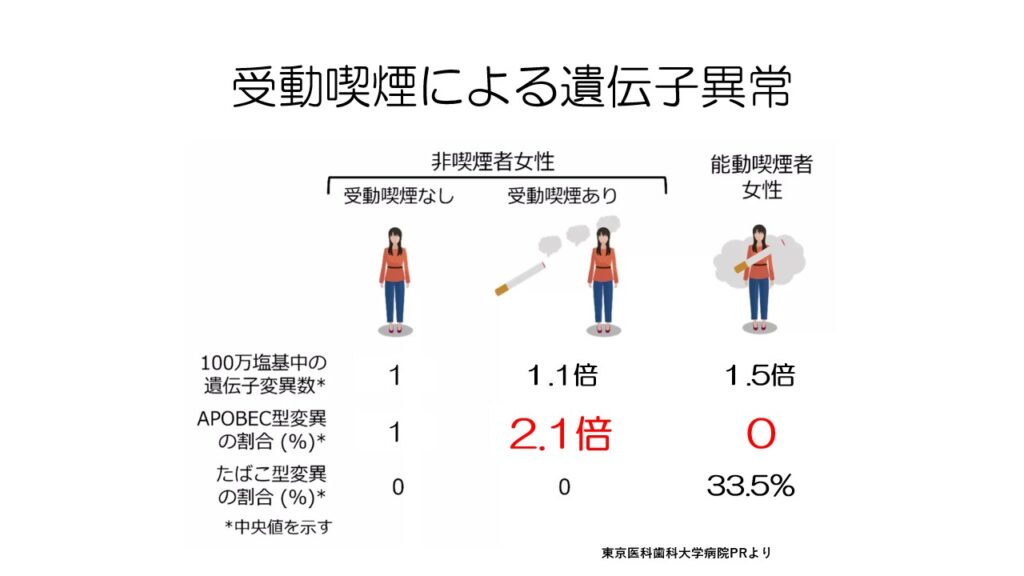
今年2024年に報告された研究ですが、受動喫煙ではAPOBEC型という肺がんの原因となる遺伝子変異が約2倍起こりやすくなるようです。
右端の喫煙者は、通常のタバコによる遺伝子変異が増えるものの、APOBEC遺伝子変異の割合はゼロとなっています。
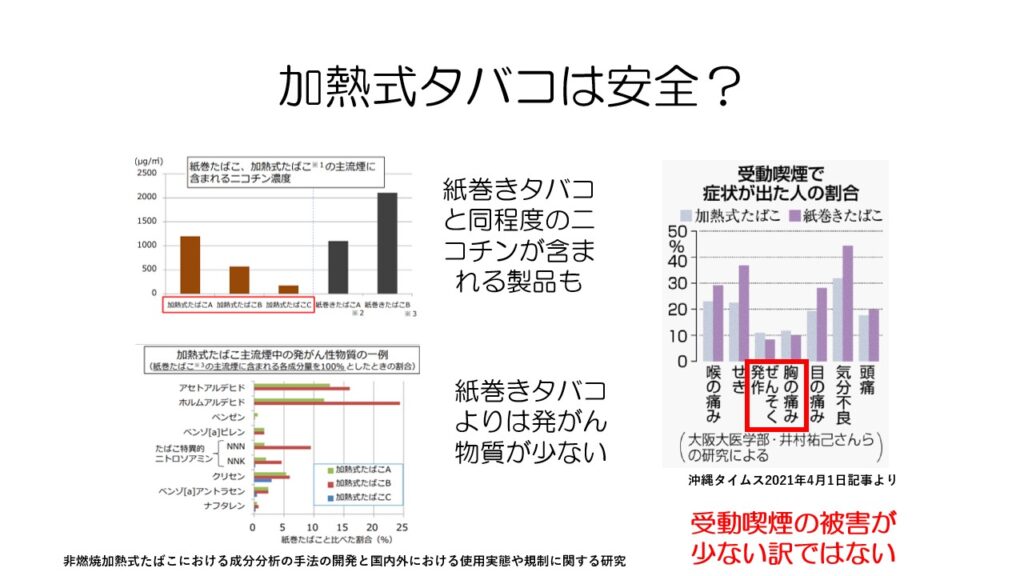
加熱式タバコは紙巻きタバコと比べて化学物質の量は少ないですが、ニコチン量が同程度の製品もあります。
また、右側のグラフを見てみると、受動喫煙による喘息発作などは紙巻きたばこよりも割合が多くなっています。
化学物質の量が少ないからと言って、受動喫煙の被害がないわけではありません。

喫煙歴のない女性の調査で、腺がんを発症した人は閉経が遅い、つまり女性ホルモンにさらされている期間が長い方がリスクが高くなることが分かりました。
肺がんの発症に女性ホルモンであるエストロゲンが関係している可能性があります。
肺がんの種類とステージ
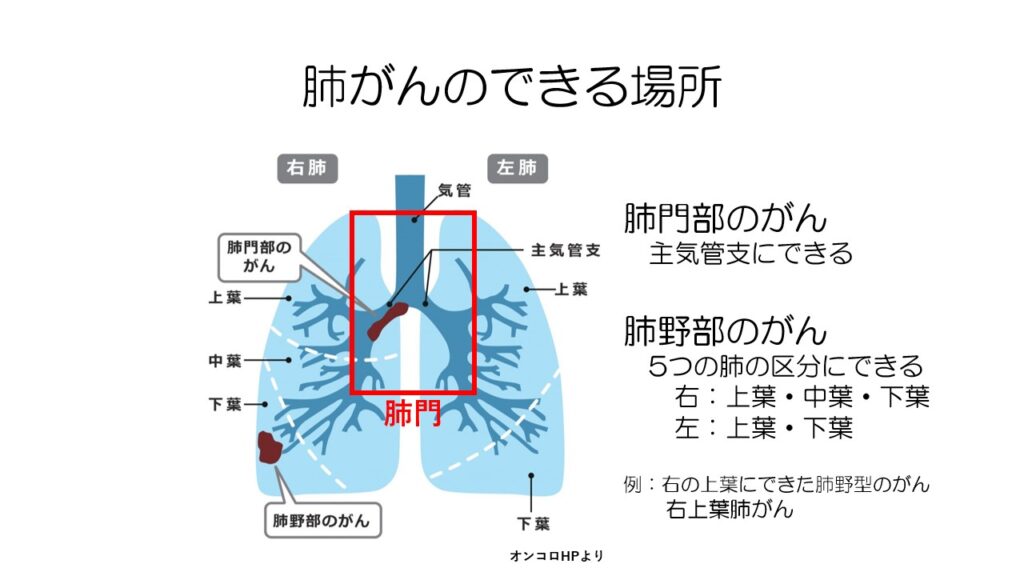
肺がんには、太い気管支にできる肺門部のがんと細い気管支や肺胞にできる肺野部のがんがあり、後述しますがそれぞれ特徴があります。
肺野部のがんは、存在位置を5つに分かれた肺の区分で表します。
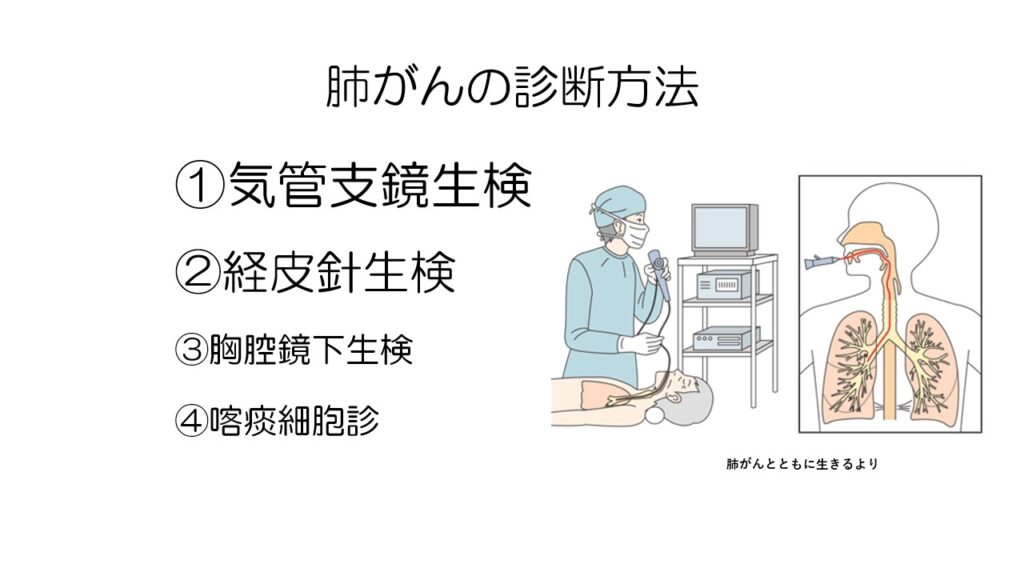
肺がんの診断を付ける方法で、最も多いのは気管支鏡を使った生検です。
気管支鏡でのぞきながら肺がんの組織を採取します。
CTで見ながら肺に針を刺す経皮針生検が行われることもあります。
①②でも診断がつかない場合には、胸腔鏡手術で肺の組織を採取します。
肺がん検診などで行われる喀痰細胞診は、肺門部のがんで有効です。
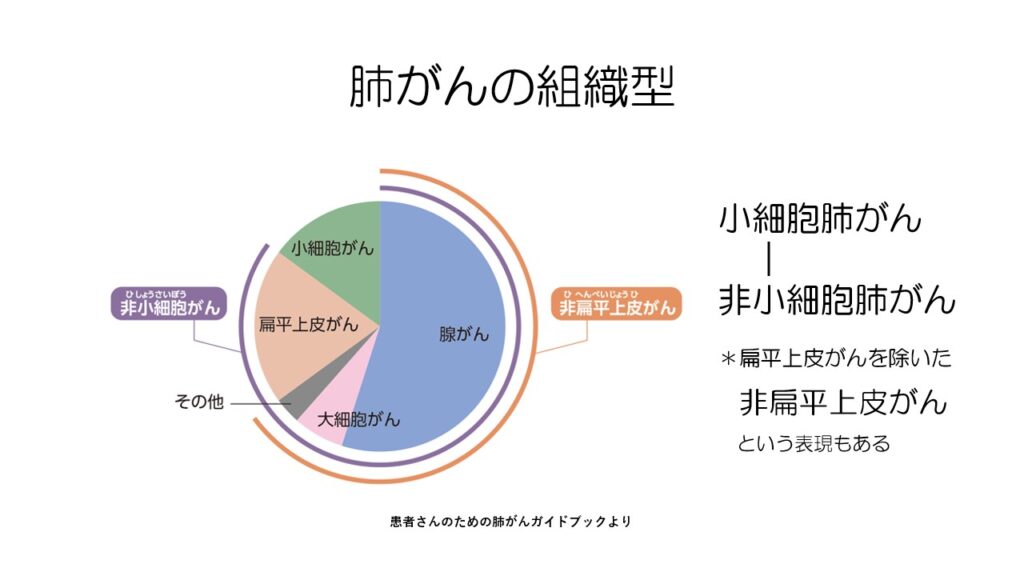
肺がんの組織型は大きく分けて、腺がん、扁平上皮がん、大細胞がん、小細胞がんの4つに分けられます。
小細胞がん以外を非小細胞がん、非小細胞がんの中で扁平上皮がんを除いたものを非扁平上皮がんと表現します。
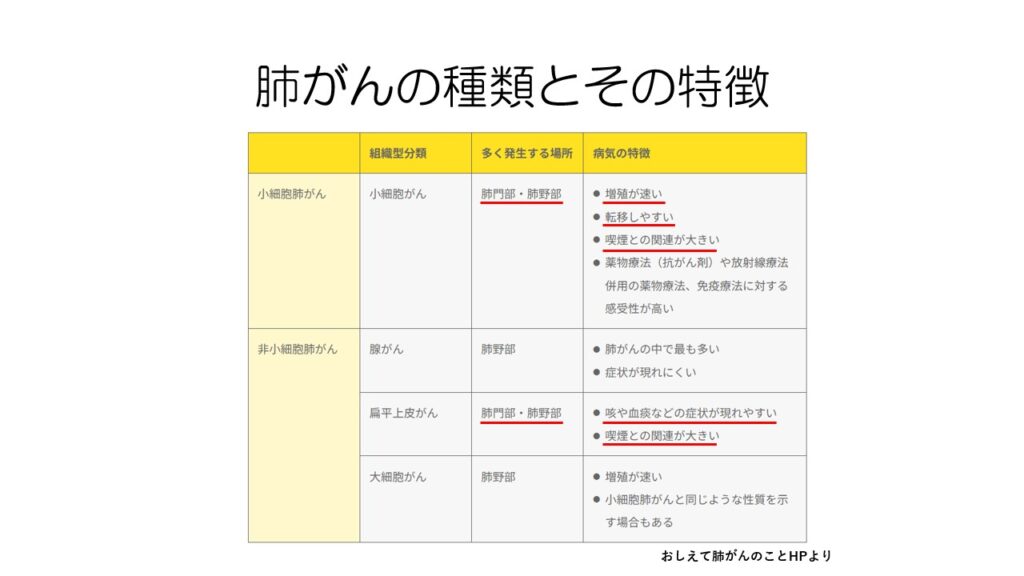
小細胞がんを特別扱いする理由は、他のタイプよりも増殖が速く転移しやすいので予後が非常に悪いからです。
治療法も小細胞肺がんと非小細胞肺がんとでは全く異なります。
また、肺門部にできやすい小細胞がんや扁平上皮がんは、喫煙との関係が強く、血痰などの症状が出やすいという特徴があります。
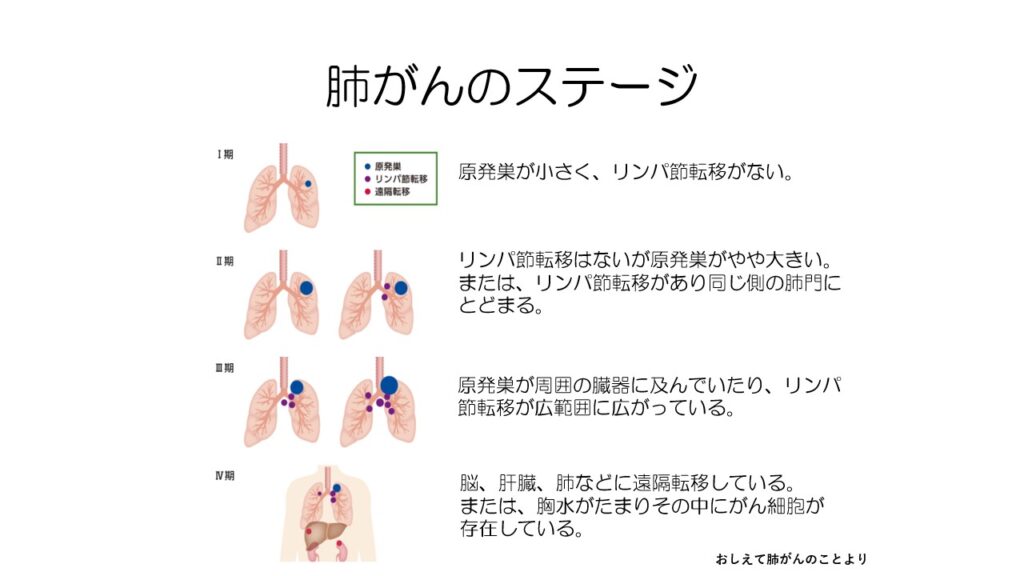
肺がんのステージ分類は、原発巣の大きさ、リンパ節転移の範囲、遠隔転移の有無で決まります。
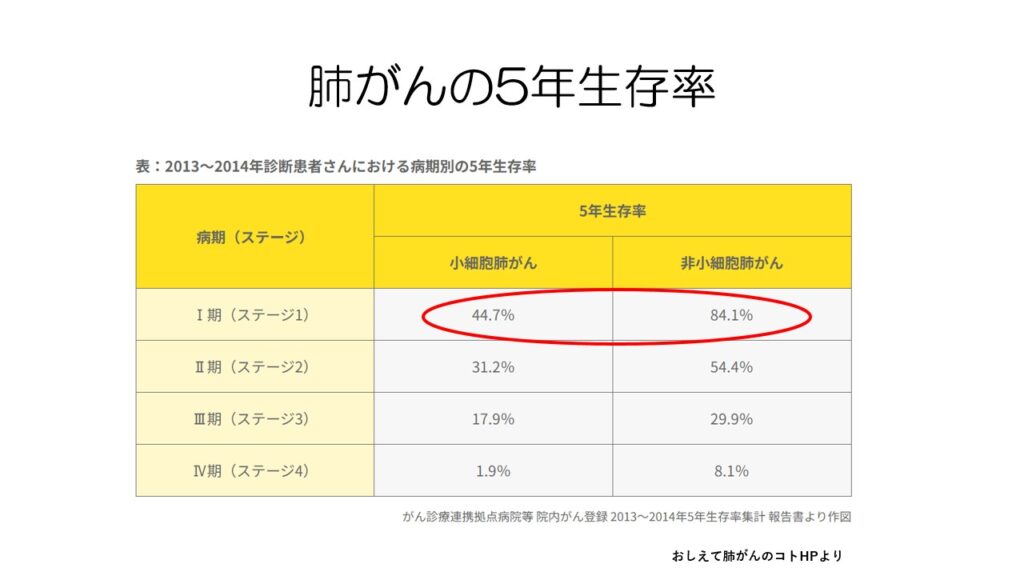
肺がんの5年生存率は、小細胞肺がんと非小細胞肺がんで大きく異なります。
ステージ1という早期でも小細胞肺がんは5年生存率が低いことが分かります。
ステージ別の治療法(非小細胞肺がん)
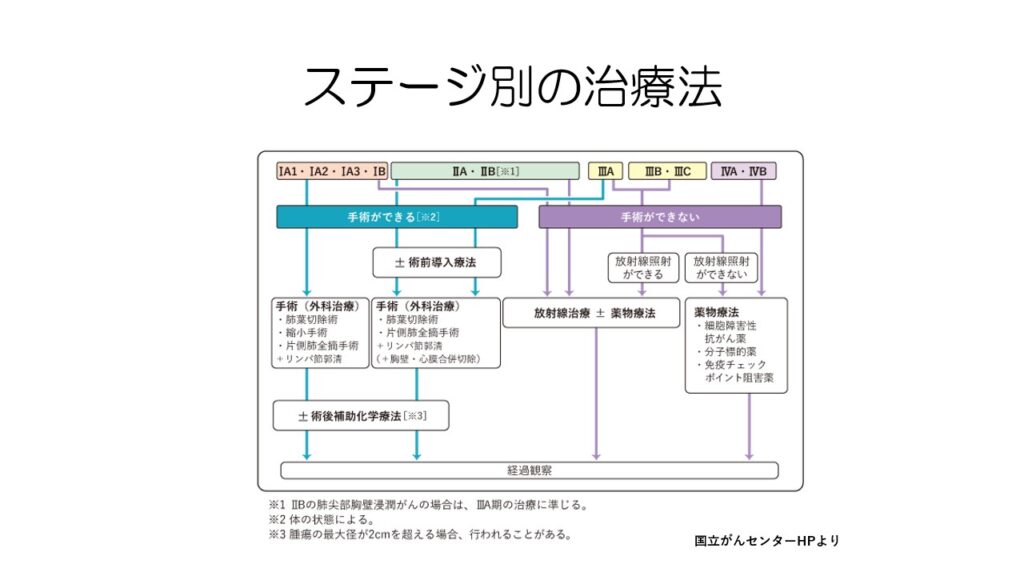
非小細胞肺がんのステージ別の治療法は、ガイドラインではこのように複雑になっています。
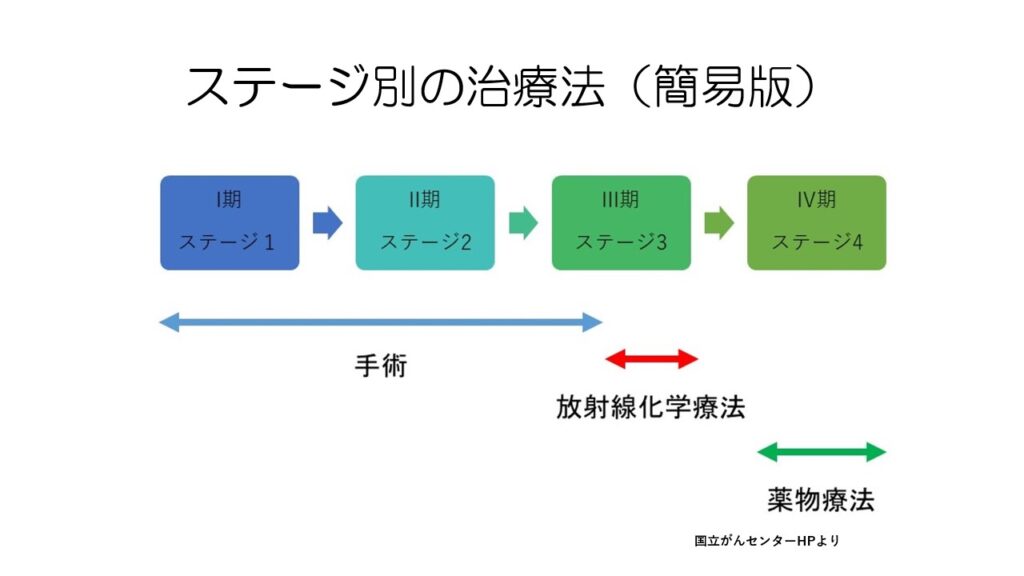
簡単にするとこんな感じです。
ステージ1から3の一部までは手術、ステージ3は放射線化学療法、遠隔転移のあるステージ4では薬物療法が行われます。
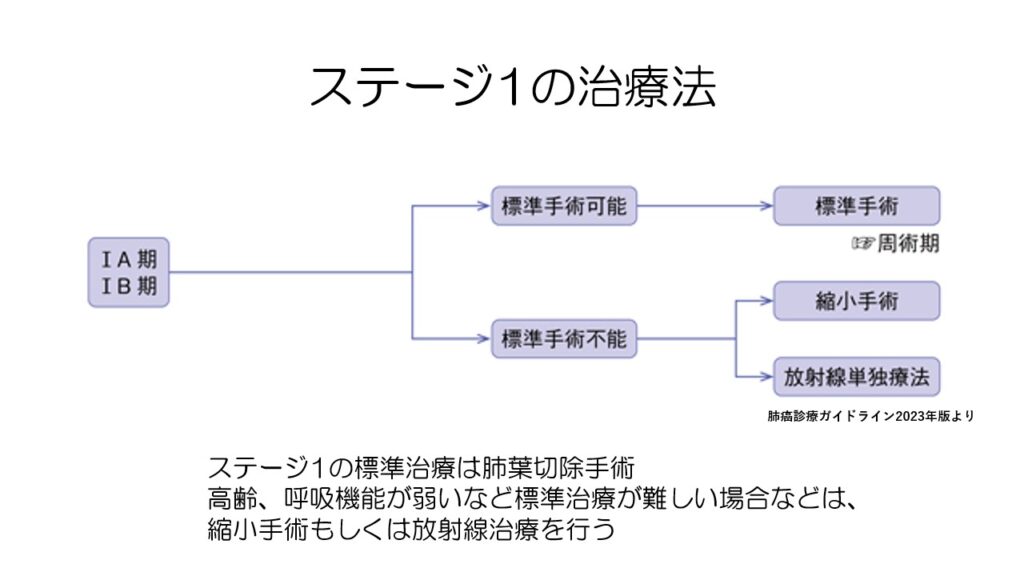
ステージ1の標準治療は手術です。
高齢や呼吸機能が弱い場合には、縮小手術もしくは放射線治療が行われます。
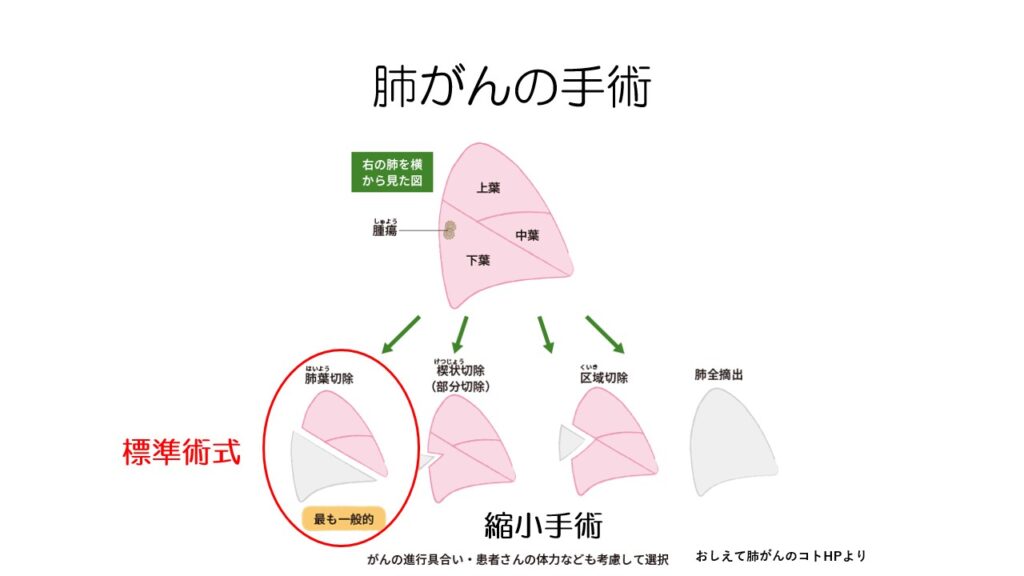
標準術式は一番左の肺葉切除です。
がんが存在している肺葉を丸ごと切除します。
呼吸機能が弱い場合などは、部分切除や区域切除を行います。
がんが全ての肺葉に広がっている場合には肺全摘出手術を行います。
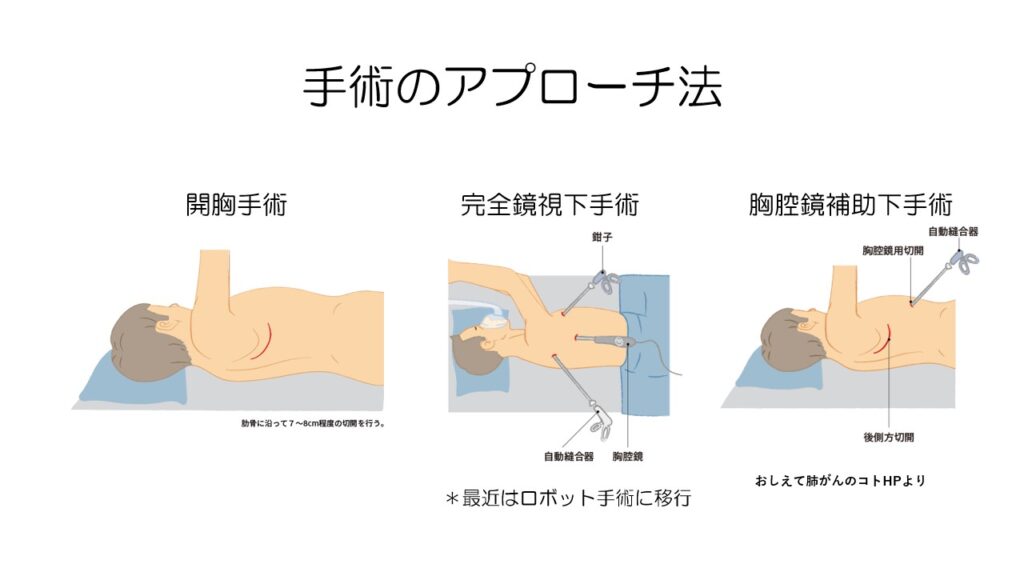
開胸手術は現在では行われることがほとんどなくなり、胸腔鏡補助下手術、もしくは完全鏡視下手術が行われます。
最近ではより切開の少ないロボット手術に移行し、手術による負担はさらに減ってきています。
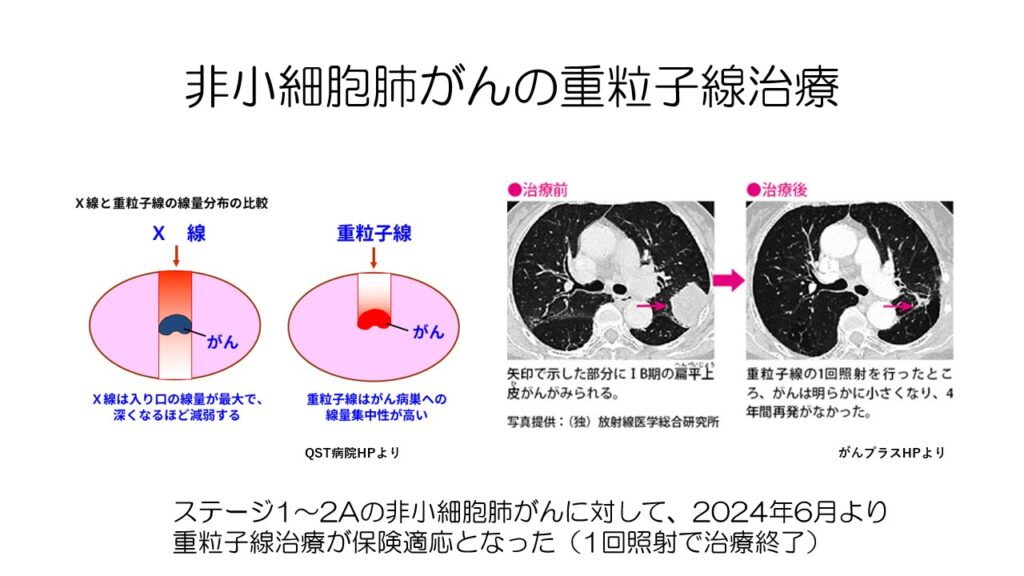
ステージ1‐2Aの非小細胞肺がんに対して、2024年6月より重粒子線治療が保険で受けられるようになりました。
通常の放射線治療より効果が高く、副作用が少ないと言う特徴があります。
また、基本的には1回照射で終了するため、通院などの負担も少なくなります。
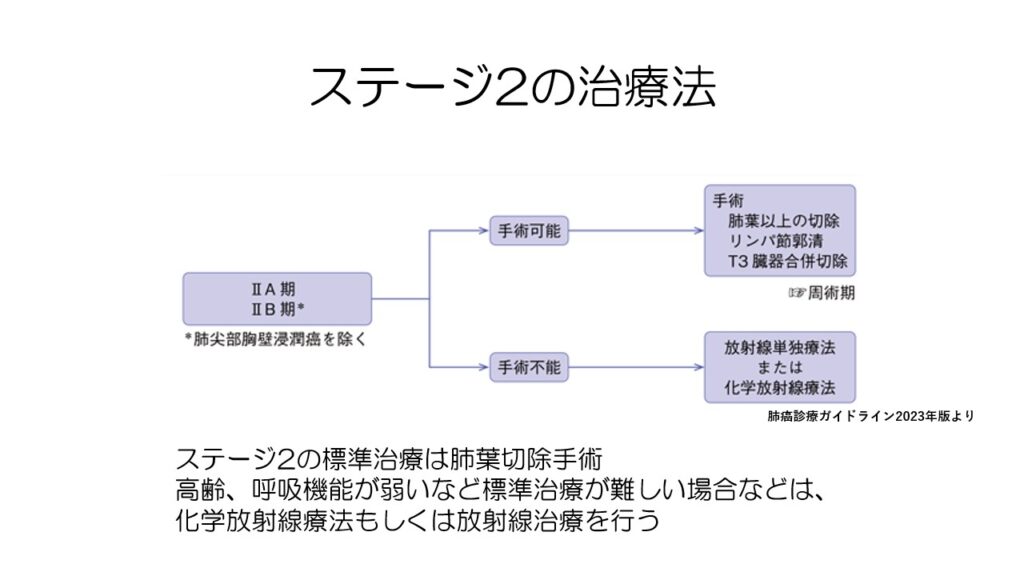
ステージ2の治療は基本的には手術です。
手術が難しい場合には、放射線治療単独か化学放射線療法が行われます。
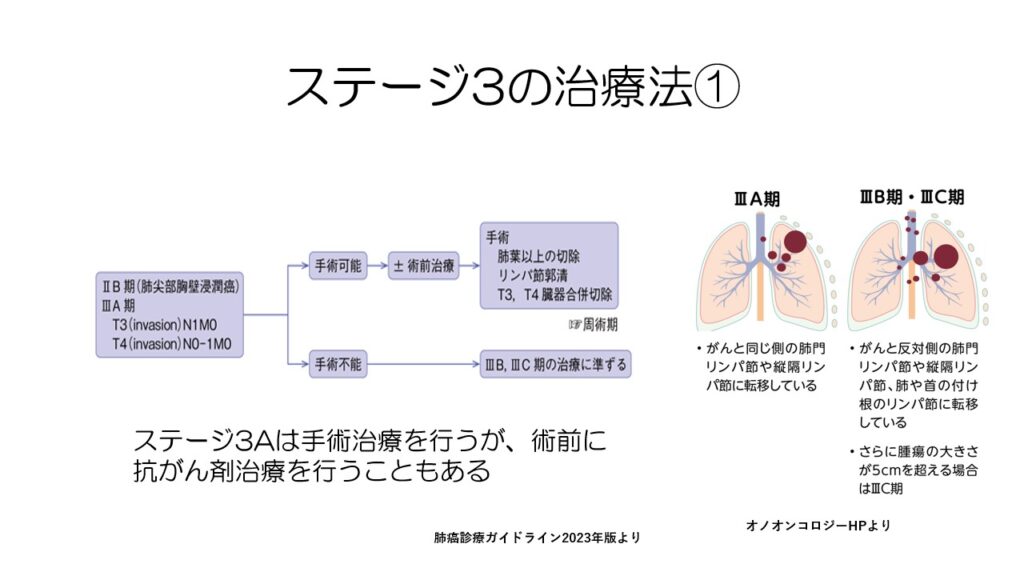
ステージ3の治療法はちょっと複雑です。
リンパ節転移が片方だけにおさまっている3Aの中で、リンパ節転移が少ない場合には手術を行ないます。手術前に抗がん剤治療を行うこともあります。
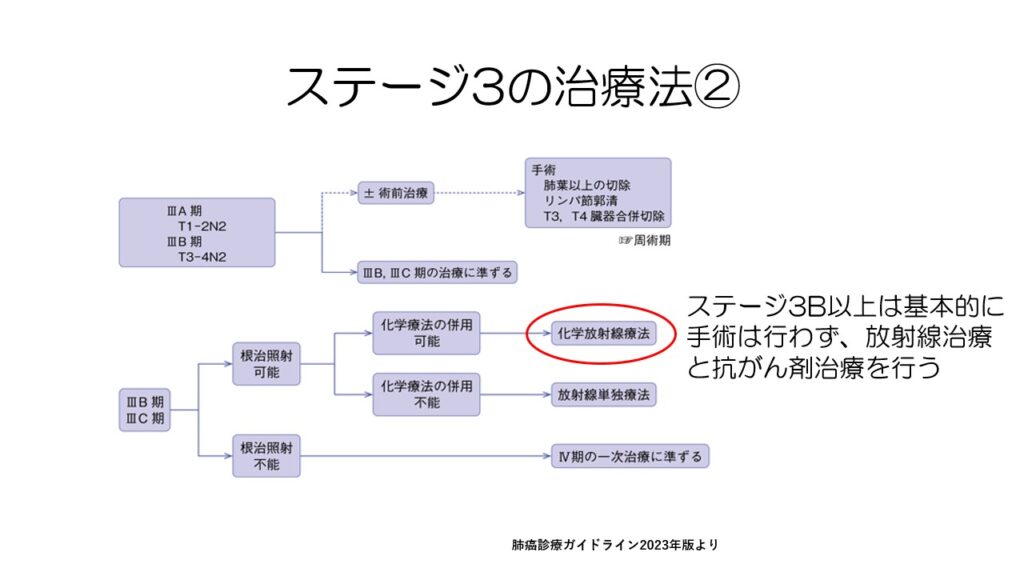
ステージ3Aでもリンパ節転移が多い場合や3B、3Cといった場合は、手術は行わず、抗がん剤と放射線治療が主となります。
この辺りを理解するのは難しいので、ステージ3と言われた人は、主治医に「ステージ3のうちのABCどれなのか」聞いてみてください。
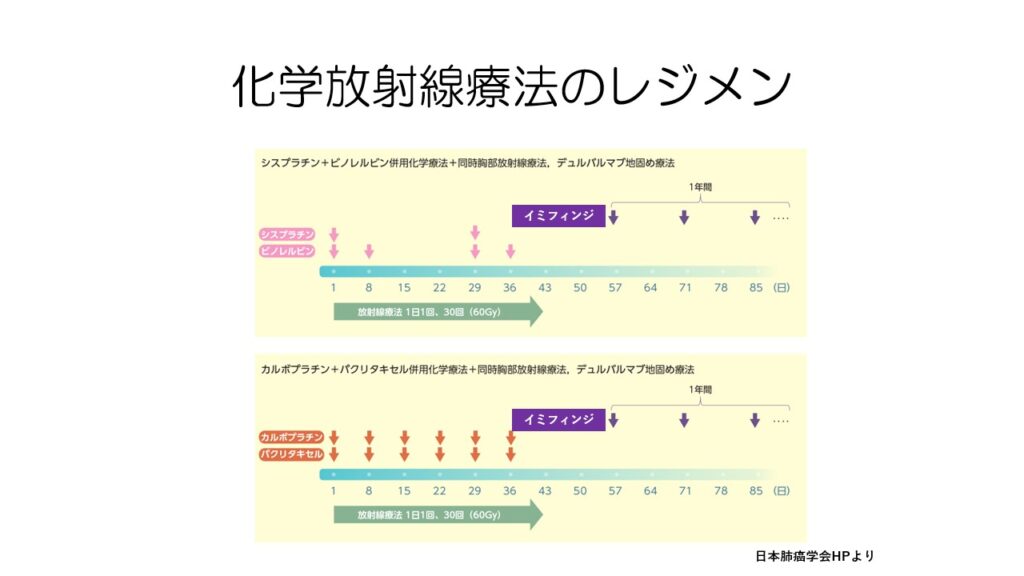
化学放射線療法は、抗がん剤治療と放射線治療を同時に行います。
その後、維持療法として1年間免疫チェックポイント阻害薬イミフィンジを投与します。
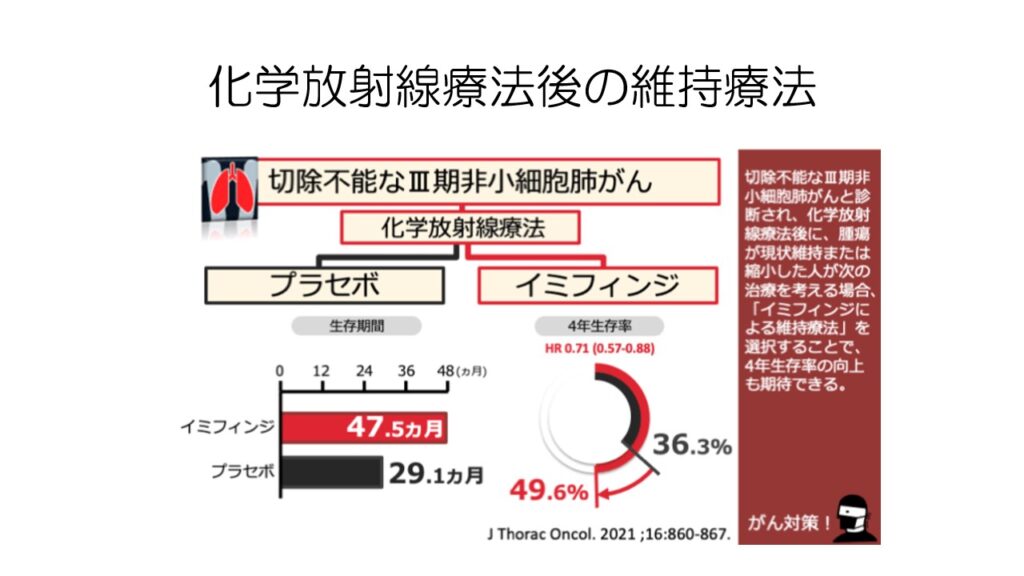
維持療法としてのイミフィンジで、生存期間が大幅に延長します。
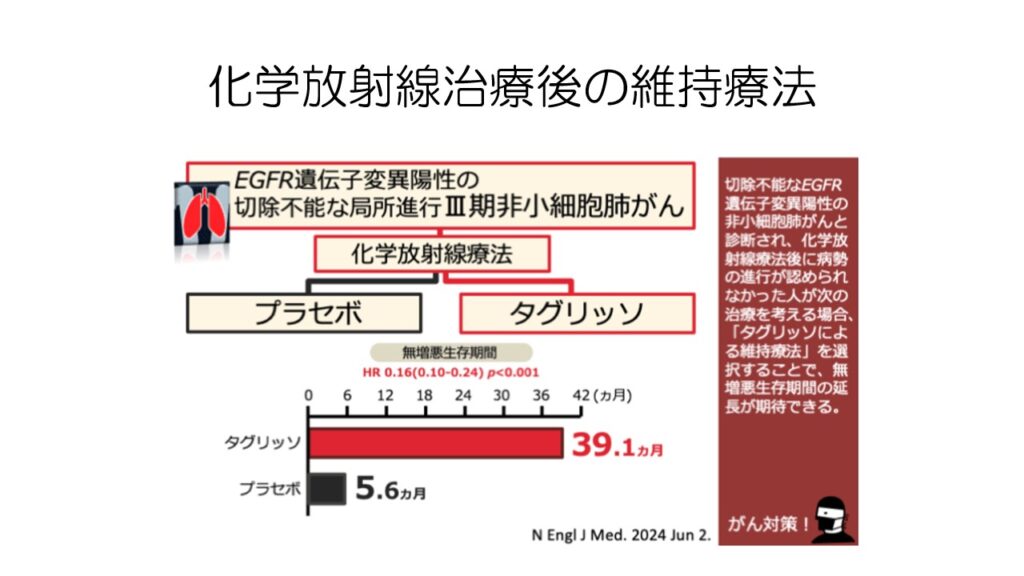
EGFR陽性であれば、ステージ3で化学放射線療法を行った後の維持療法として、タグリッソが承認待ちの状態です。
こちらも大幅に生存期間を延長します。
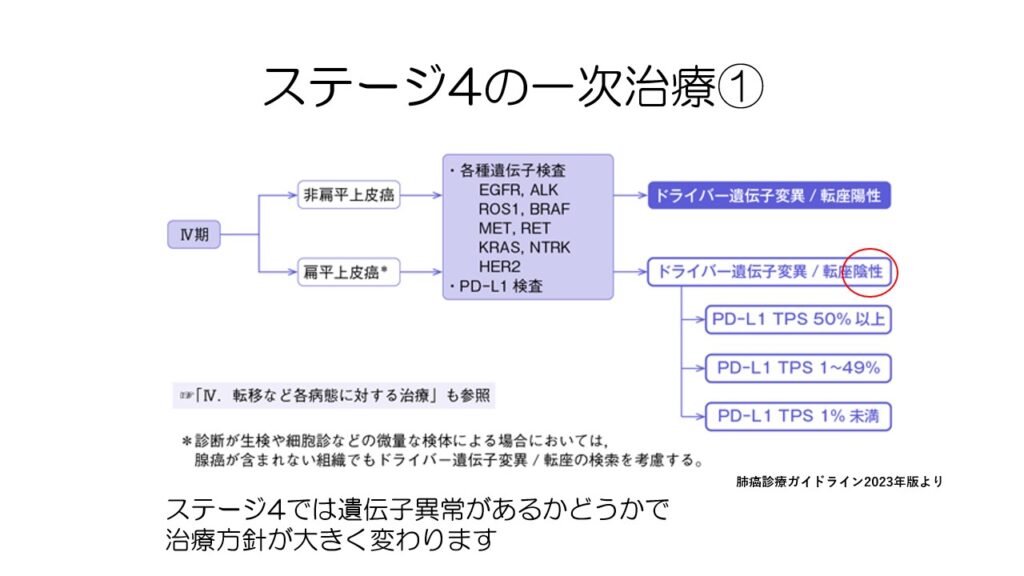
ステージ4の治療法は手術や放射線治療は行わず、薬物療法のみです。
ドライバー遺伝子の異常の有無、PD-L1の程度で選択する薬物が決定します。
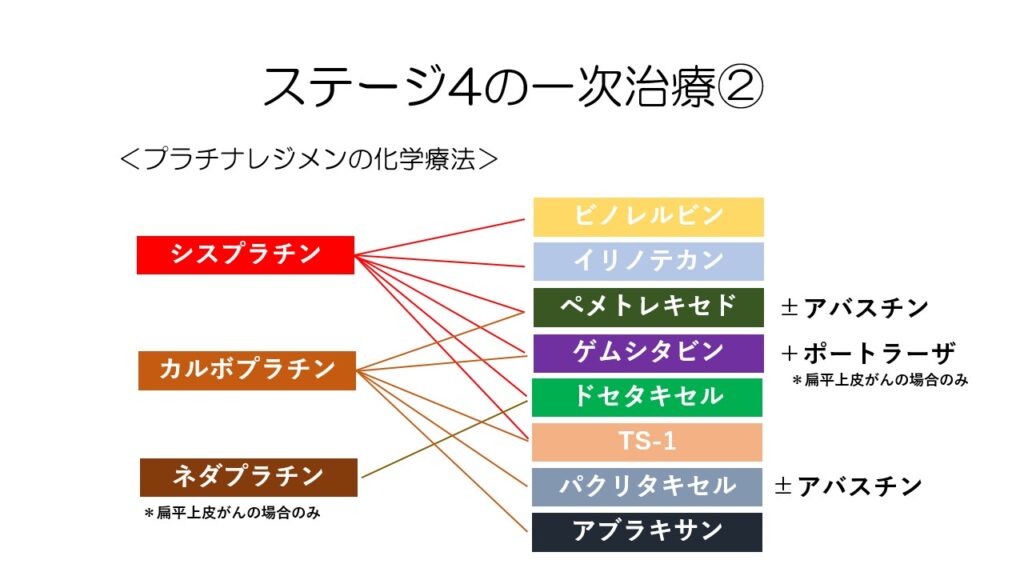
化学療法単独で行う場合にはシスプラチン・カルボプラチン・ネダプラチンなどのプラチナ系抗がん剤に他の種類抗がん剤とアバスチンなどを加えたレジメンで治療を行います。
ドライバー遺伝子陰性の場合

PD-L1の発現強度(発現量)が50%以上という強発現の場合は、免疫チェックポイント阻害薬がよく効くので、キイトルーダもしくはテセントリクの単剤療法でも良いですし、化学療法を併用しても構いません。

発現強度が1-49%の場合は、免疫チェックポイント阻害薬はプラチナ系抗がん剤もしくはオプジーボ+ヤーボイという免疫チェックポイント阻害薬の組み合わせが推奨されています。

PD-L1の発現強度が1%未満、つまり陰性の場合でも、弱陽性の場合とほぼ同じ、免疫チェックポイント阻害薬+化学療法が推奨されています。
ドライバー遺伝子養成の場合
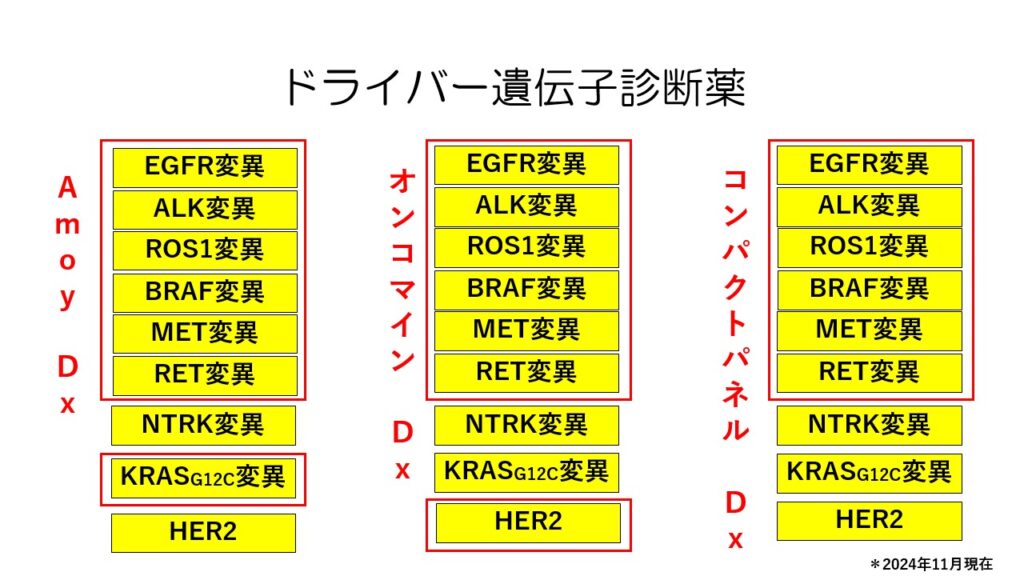
肺がんのドライバー遺伝子の異常を幅広く調べる検査が3種類あります。
始めの生検で調べることができます。
下の3つの異常は二次治療以降に遺伝子パネル検査で診断しますが、一部は初めの診断時に調べることができます。
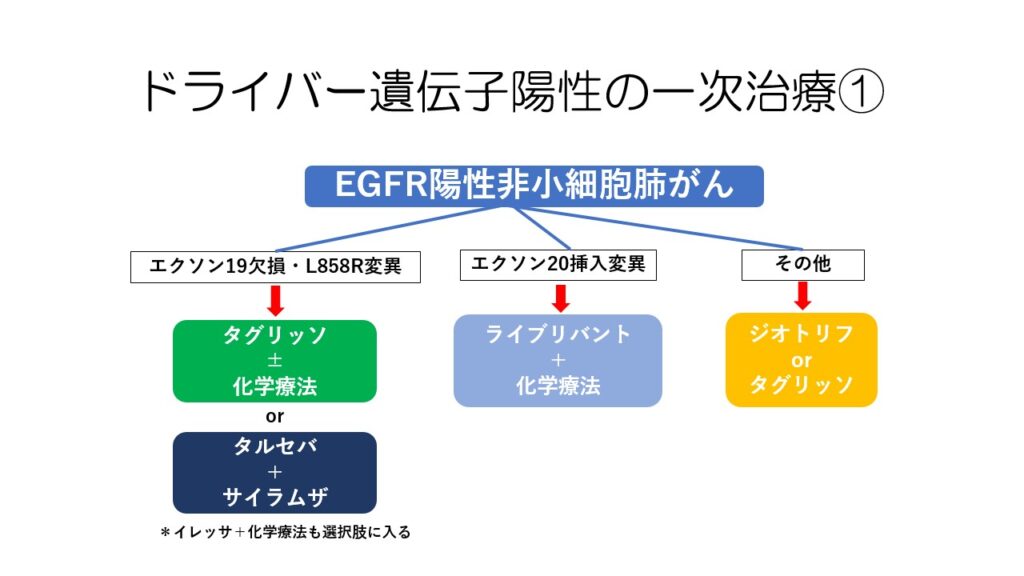
EGFR変異はドライバー遺伝子異常の中でも最も多く見られます。
EGFR遺伝子変異の中でもいくつか種類があり、それによって選択する薬剤が異なります。
エクソン20挿入変異に対するライブリバントは2024年9月に承認されたばかりです。
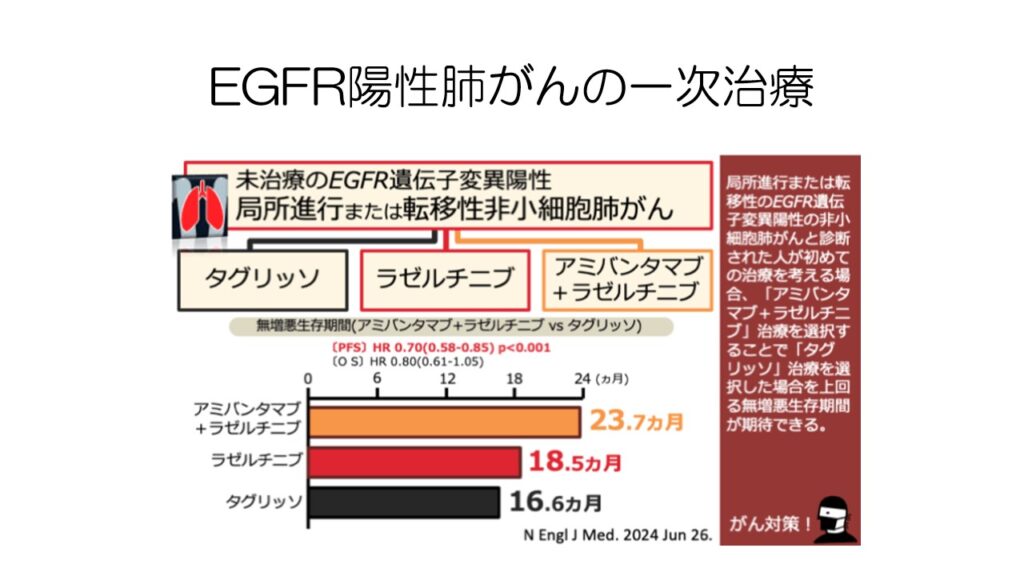
EGFR陽性で、ライブリバント(アミバンタマブ)+ラゼルチニブの併用療法が承認待ちの状態です。
先ほどの一次治療のフローが今後大きく変わりそうです。
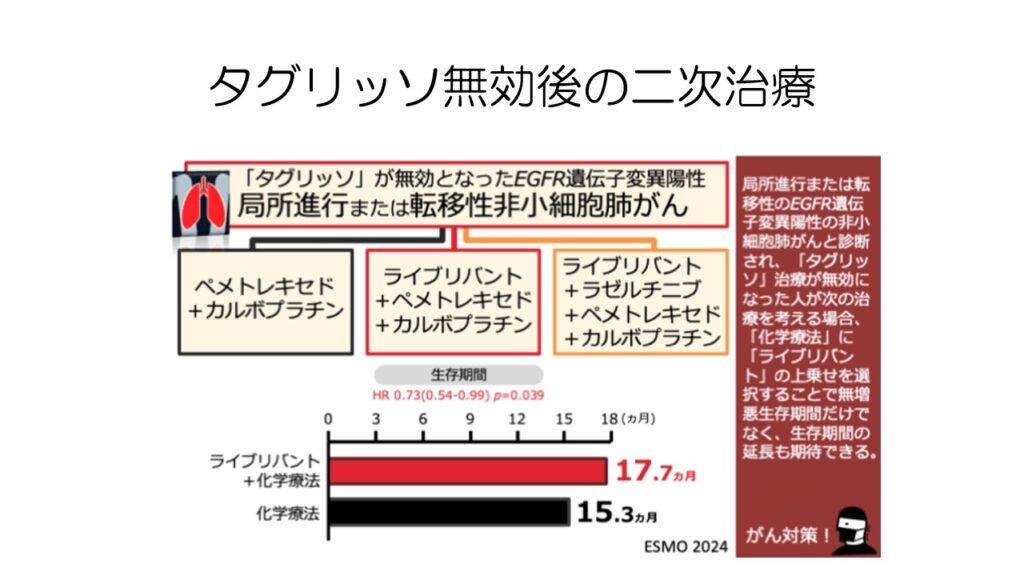
また、タグリッソが無効となった後は、これまで化学療法を行う以外方法はありませんでしたが、ライブリバント+化学療法が承認申請されました。

EGFR以外のドライバー遺伝子に対して、様々な薬剤が開発されています。
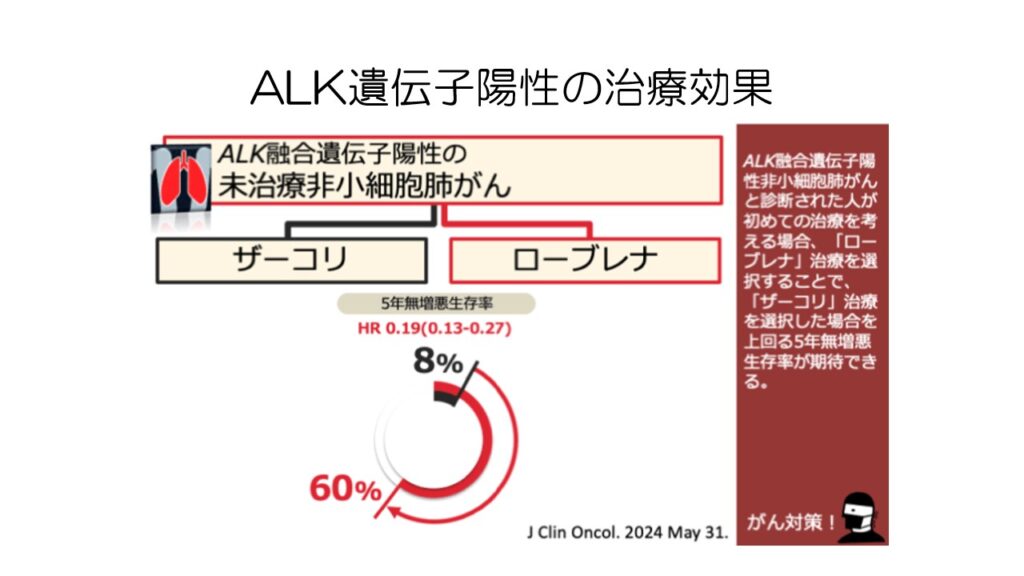
ALK遺伝子変異に対する新薬ローブレナは、5年無再発生存期間が60%となっています。
これは、ALK陽性のステージ4の肺がんで、60%の人が5年経ってもがんが増悪していないということです。

こちらの3つの遺伝子異常に対しての分子標的薬は、二次治療以降で使用されます。
診断も主に遺伝子パネル検査で行われます。
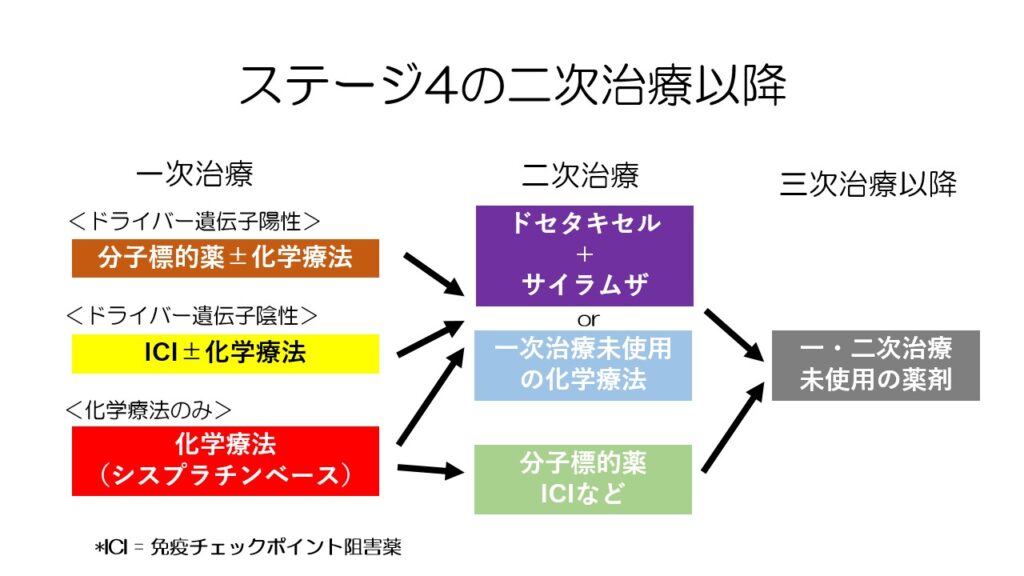
二次治療以降のまとめです。
基本的に免疫チェックポイント阻害薬は一度のみ使用しますし、分子標的薬は適応する変異があれば二次治療以降でも使用できます。
こちらも詳細は銀座みやこクリニックのアメーバブログで解説しておりますので、ぜひご覧ください。
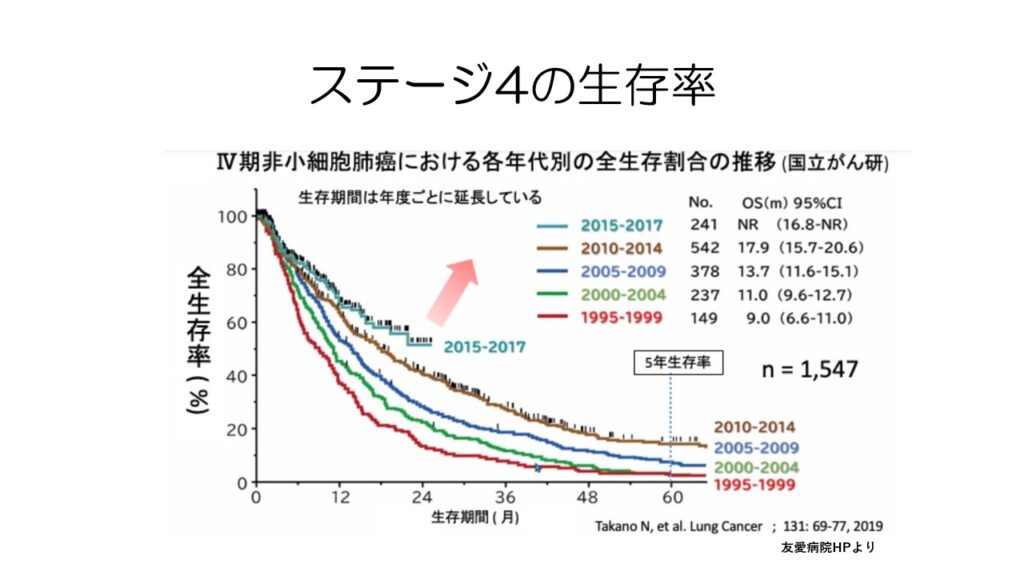
薬物療法の進歩により、ステージ4の生存率が年々上昇してきています。
個別化医療がもっと進めば、5年生存率が30%を超える日も近いかもしれません。
術前・術後化学療法(非小細胞肺がん)

ステージ2Aまでの肺がんでは、手術後に抗がん剤UFTを2年間内服します。ステージ1で腫瘍径が2㎝以上の場合に抗がん剤の効果が見られます。
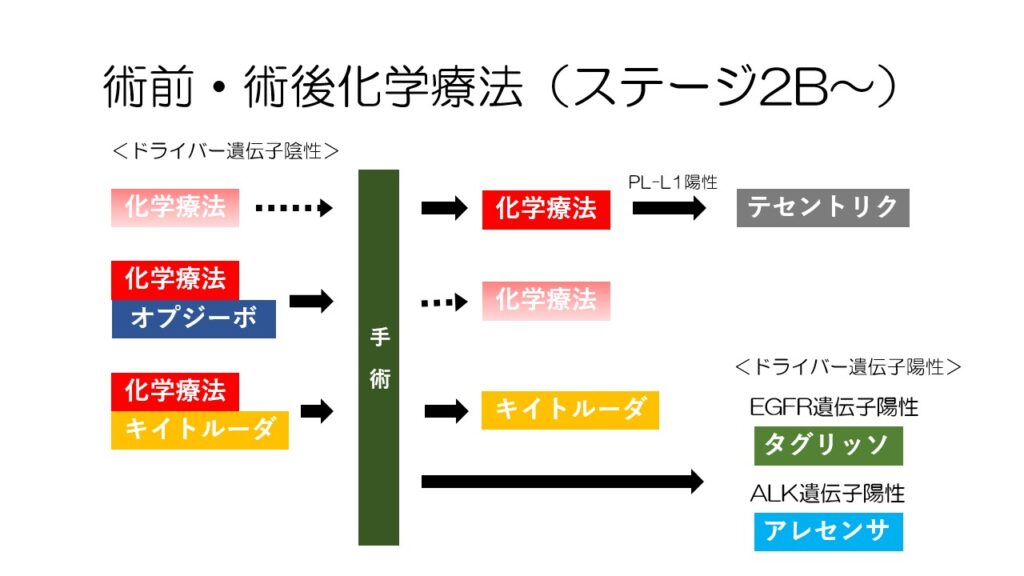
ステージ2B以上の場合、このような術前・術後治療が行われます。
この辺りは銀座みやこクリニックのブログで詳しく解説していますので、ぜひご覧ください。
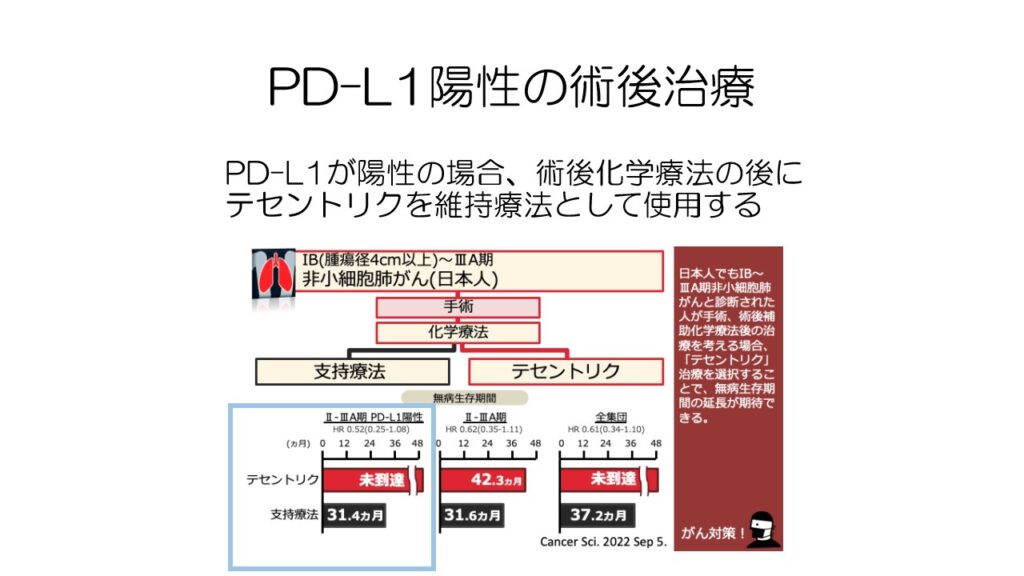
PD-L1陽性の場合には、化学療法の後に免疫チェックポイント阻害薬テセントリクを1年間投与します。
無再発期間の延長が期待できます。
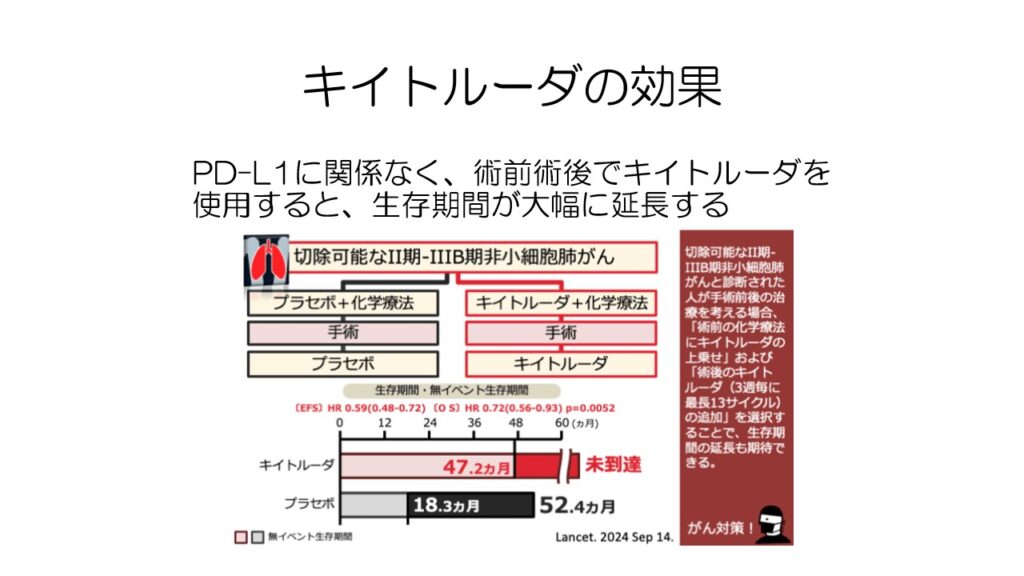
2024年8月にキイトルーダが術前術後治療で承認されました。
術前は化学療法と併用し、術後はキイトルーダ単独で投与します。
無再発期間が4年弱で、生存期間は5年を超えています。
こちらはPD-L1に関係なく投与が可能です。

ドライバー遺伝子に異常があることが分かれば、術前治療は行わずに、術後に分子標的薬を投与します。
手術単独よりも高い生存率が期待できます。
ステージ別の治療法(小細胞肺がん)
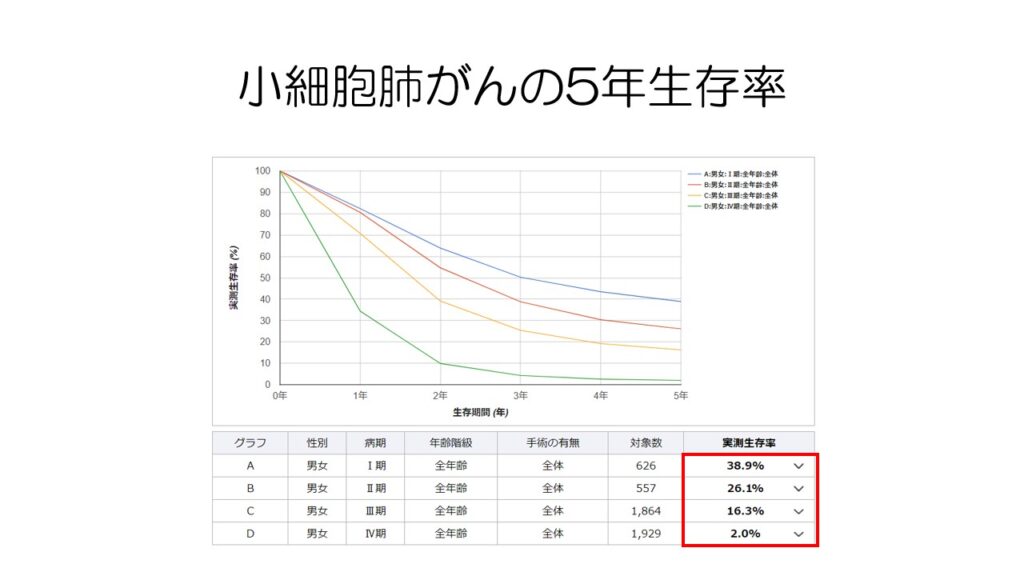
小細胞肺がんは非小細胞肺がんと比べて生存率がかなり低下します。
ステージ1でも5年生存率が40%を切っており、ステージ4に至っては2%しかありません。
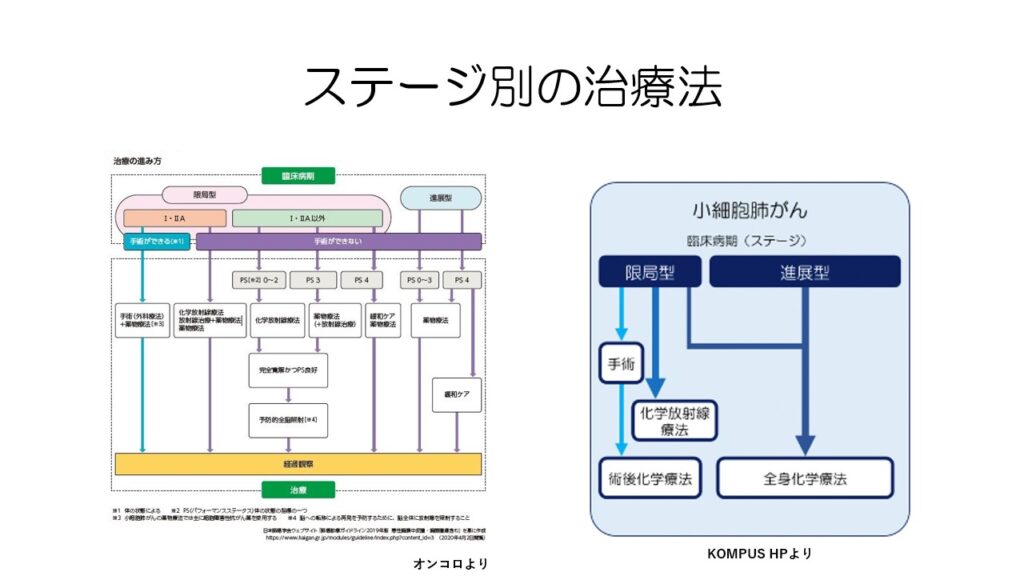
そんな、なかなか予後が厳しい小細胞肺がんですが、非小細胞肺がんよりは治療法がシンプルです。
ステージ別と言うよりは、ステージ1-3を「限局型」、ステージ4を「進展型」と表現し治療法を判断します。
小細胞肺がんは進展型であるステージ4で発見されることが多く、限局型は20%ほどしかありません。

限局型のうち、ステー1と2Aの場合のみ、手術が可能です。
ステージ1の5年生存率は約40%ですが、手術で完全切除できた場合には70%まで上がります。
また、ステージ2の5年生存率は26%ですが、手術で完全切除できた場合には50%まで上がります。
予後が悪い小細胞肺がんといえども、早期で発見して手術ができれば生存率の改善が期待できます。
手術後には抗がん剤治療が必須です。
手術ができない場合には、化学放射線療法が行われます。

限局型小細胞肺がんの化学放射線療法後に、維持療法として免疫チェックポイント阻害薬イミフィンジを投与することで、生存期間を延長させるという臨床試験がありました。
現在承認待ちの状態です。
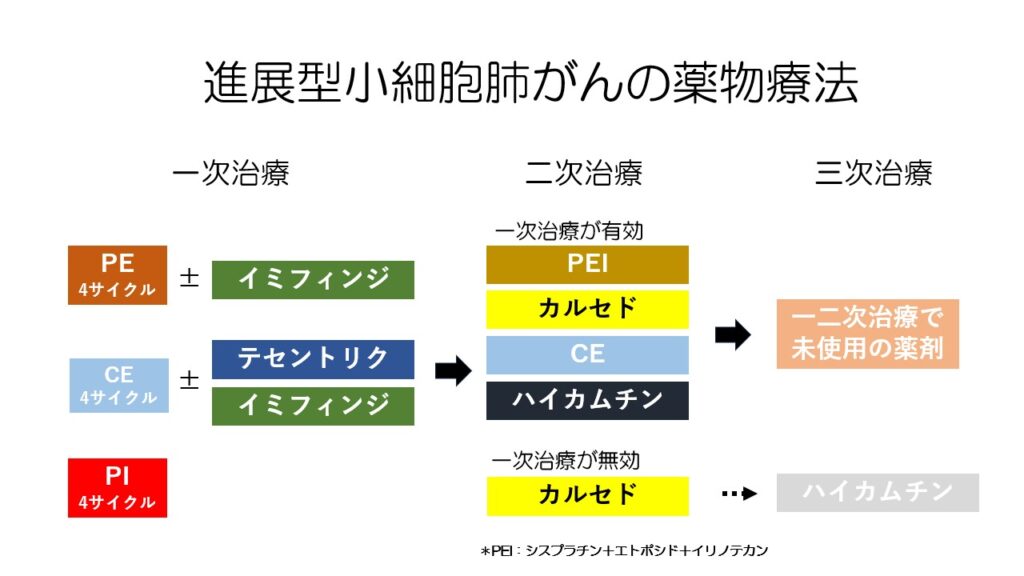
一次治療では、化学療法+免疫チェックポイント阻害薬が現在標準治療となっています。
一次治療は20年以上化学療法だけだったのが、2019年にテセントリク、2020年にイミフィンジが承認されました。
一次療法の化学療法は、基本的には4サイクルのみ行い、その後はテセントリクやイミフィンジを無効となるまで継続します。
一次治療の化学療法が終了し、再発までの期間によって一次治療の効果を判定します。
治療終了から60~90日以上経過している場合、一次治療が有効だったと判断し、治療終了から60~90日以内の場合には一次治療が無効だったと判断します。
それにより二次治療が異なります。
三次治療以降は、一二次治療で使用されていない薬剤が使われます。
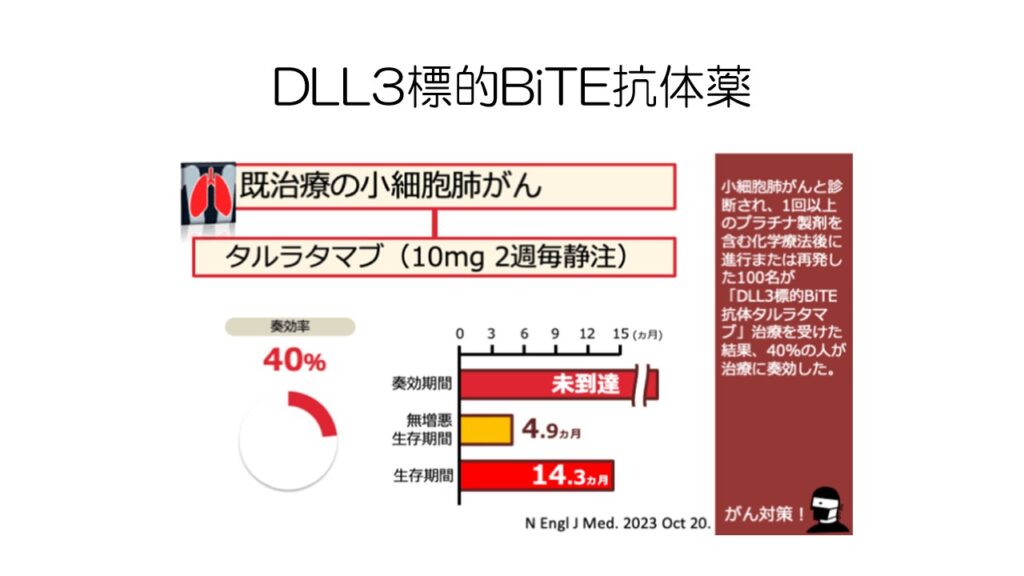
進展型小細胞肺がんの二次治療以降の薬剤として、タルラタマブという薬剤が承認申請されています。
一次治療で免疫チェックポイント阻害薬が登場したものの、二次治療以降では長らく新薬が登場しなかったので、やっと選択肢が増えそうです。
肺がん治療のまとめ
- 肺がんの治療薬はこの10年で数多くの新薬が登場し、ドライバー遺伝子陽性のステージ4肺がんでも5年生存する症例が増えてきている。
- 難治性の小細胞肺がんも免疫チェックポイント阻害薬の登場で、長期生存例が増えてきた。
- 肺がんの薬物療法は「 1年前のガイドラインの情報は古い」というくらい新陳代謝が激しいので、常に最新の情報を得るようにして欲しい。
- 2024年10月現在の最新治療についてまとめたが、1年以内に諸所変更される可能性がある。




















コメント