
【PARTNER試験】小児がんでも諦めない

 濱元誠栄院長
濱元誠栄院長こんにちは、銀座みやこクリニック院長の濱元です。
先日、Xのこんな投稿を見つけました。
DIPG(びまん性橋膠腫)は小児の脳幹部(橋:きょう)に好発する悪性の腫瘍です。
その治療薬であるOP-10(アメリカではONC201)が、PARTNER試験の対象となる薬剤に追加されたというものです。
今回は、PARTNER試験について解説していきます。
PARTNER試験とは?
2024年1月の国立がん研究センターのプレスリリース
小児・AYA世代がん患者のドラッグアクセスの改善を目指す複数の適応外薬、未承認薬を対象とする医師主導臨床研究開始
患者申出療養制度というのがあります。
詳しくは厚生労働省のサイトを参照に 厚生労働省 患者申出療養制度
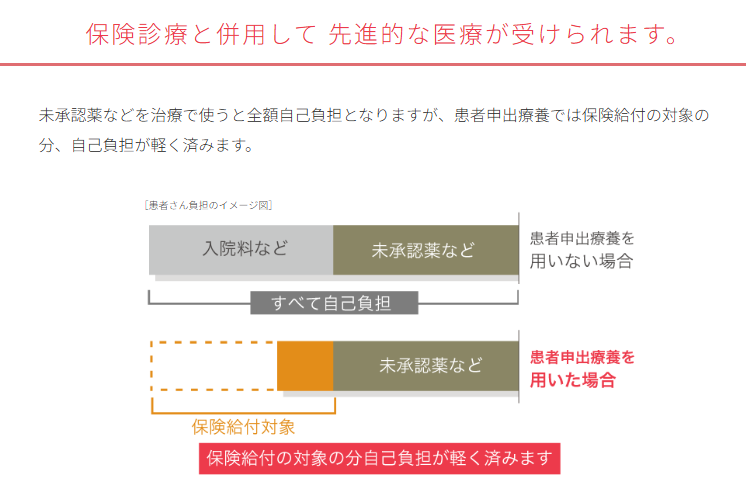
通常、未承認薬や未承認手術などの保険適応外の治療すると、薬剤や手技料以外の診療費や入院費なども保険適応外となりますが、この制度を利用すると薬剤費以外は保険適応になります。
ただ、この制度にはいろいろと制約があります。
- 特定の薬剤や手技でのみ利用可能
- 一定数(30-50人)に達したら終了
- 特定の医療機関でのみ実施
使用したい薬剤が患者申出療養制度の適応でなければその薬剤は使えませんし、定員になってしまうと制度の適応外となります。
また、医療機関も限られていて、例えば以下のように全国で1か所のみということもあります。
| EPI―589経口投与療法 筋萎縮性側索硬化症(過去にEPI―589が投与された患者に係るものに限る。) | 大阪府 | 大阪大学医学部附属病院 |
表題にあったPARTNER試験は、
小児やAYA世代など30歳未満で遺伝子パネル検査結果等に基づく複数の分子標的治療
が制度の対象となっていて、2024年1月から開始されました。
PARTNER試験は簡単に言うと、成人用の薬剤を小児で使おうというものです。
小児がんは成人のがんよりも遺伝子変異の頻度が高く、遺伝子パネル検査で使用できる薬剤が見つかる可能性が高いと言われています。
それなのに、日本では数の少ない小児がんでは分子標的薬の小児での治験が進まず、分子標的薬が適応となっていないことがほとんどです。
海外では承認・もしくは治験で良い結果が出ている薬剤で、基本的に日本国内でも販売されている薬剤が治験の対象となります。
そして、製薬メーカーが薬剤を無償で提供するというのも大きな特徴です。
PARTNER試験の対象となる薬剤と施設
グリベック®錠(一般名:イマチニブメシル酸塩)
ヴォトリエント®錠 (一般名:パゾパニブ塩酸塩)
メキニスト®錠 (一般名:トラメチニブ ジメチルスルホキシド付加物)
メキニスト®小児用ドライシロップ(一般名:トラメチニブ ジメチルスルホキシド付加物)
テセントリク®点滴静注(一般名:アテゾリズマブ)
カボメティクス®錠 (一般名:カボザンチニブリンゴ酸塩)
エザルミア®錠(一般名:バレメトスタットトシル酸塩)
ザーコリ®カプセル (一般名:クリゾチニブ)
OP-10カプセル ←2025年4月追加
*1薬剤当たり最大30人まで
国立がんセンター中央病院
九州大学病院
北海道大学病院
岡山大学病院
名古屋大学病院 ←2025年4月追加
遺伝子パネル検査で上記の薬剤がHitした場合は、ぜひこのPARTNER試験を利用してください。
1薬剤につき30名程度の定員があるので、主治医と相談し、早め早めに動いた方がよいです。



















コメント