
大腸がん治療完全ガイド/新薬/ステージ別治療法/分子標的薬/免疫チェックポイント阻害薬/遺伝子検査
【YouTube動画でご覧になりたい方はこちら】
 濱元誠栄院長
濱元誠栄院長こんにちは、銀座みやこクリニック院長の濱元です。
今回は大腸がん治療完全ガイドというテーマでお話させていただきます。
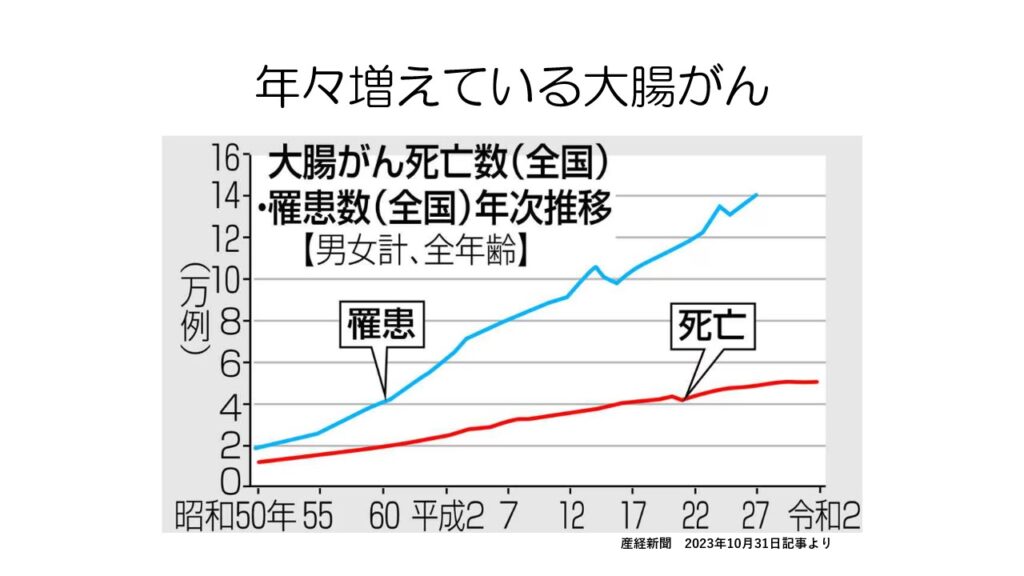

大腸がんは罹患者数と死亡者数ともに右肩上がりで増えています
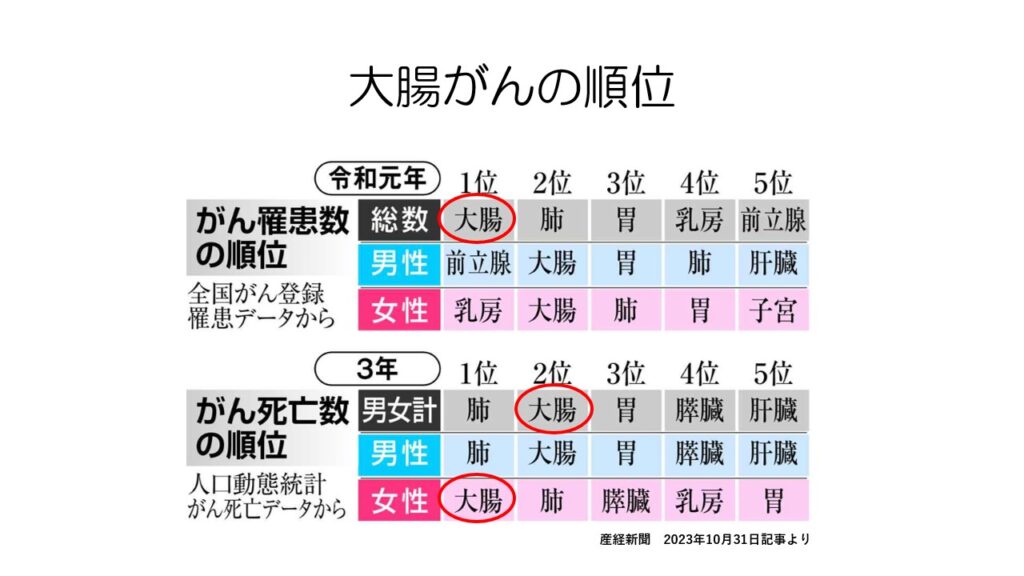

罹患者数は男女ともに2位で合わせると1位に、死亡者数は女性では1位で総合すると2位となっています。
大腸がんは、がん全体の中でも罹患者数も死亡者数も多いがんと言えます。
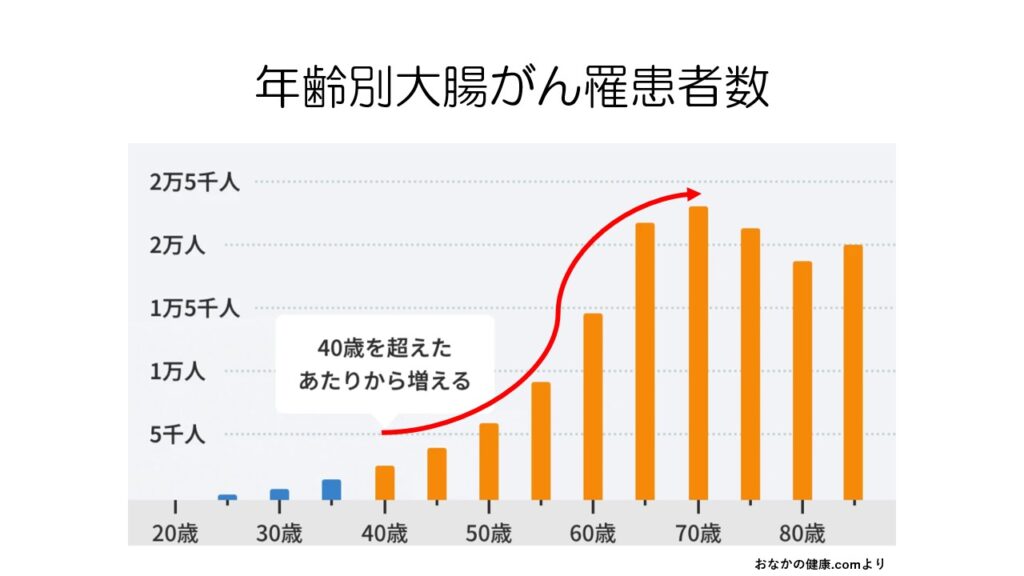

年齢別に見た大腸がんの罹患者数のグラフです。高齢者で多くみられます。
20代30代で大腸がんになる人もいますが、まだ少なく、40歳以降から増え始めます。
大腸がんの症状
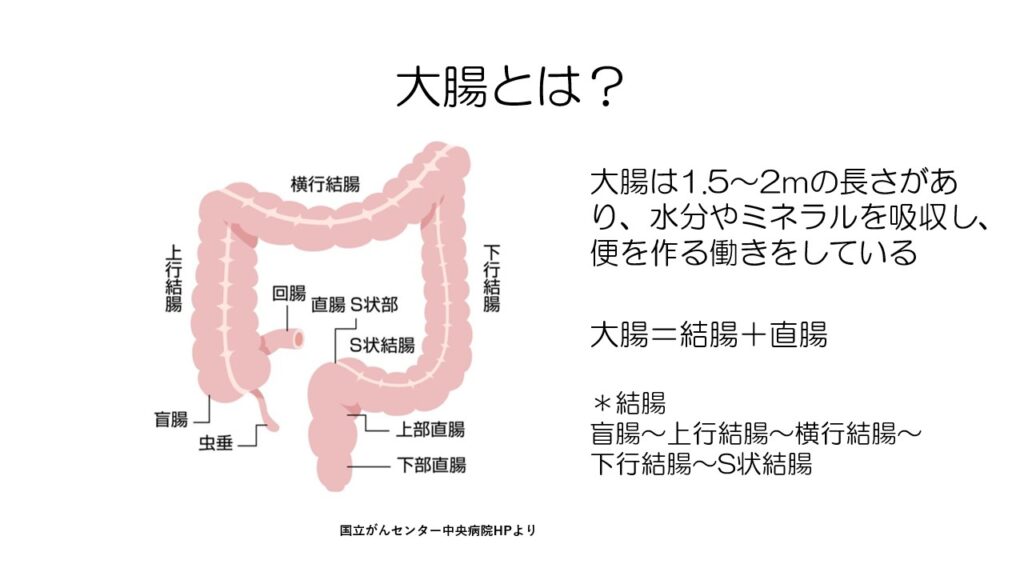

大腸は1.5~2mの長さがあり、水分やミネラルを吸収して便を作る働きをしています。
大腸は結腸と直腸からなり、結腸は盲腸からS状結腸に分かれます。
一言で大腸がんと言っても、後述しますが、できた部位によって治療法が若干異なります。
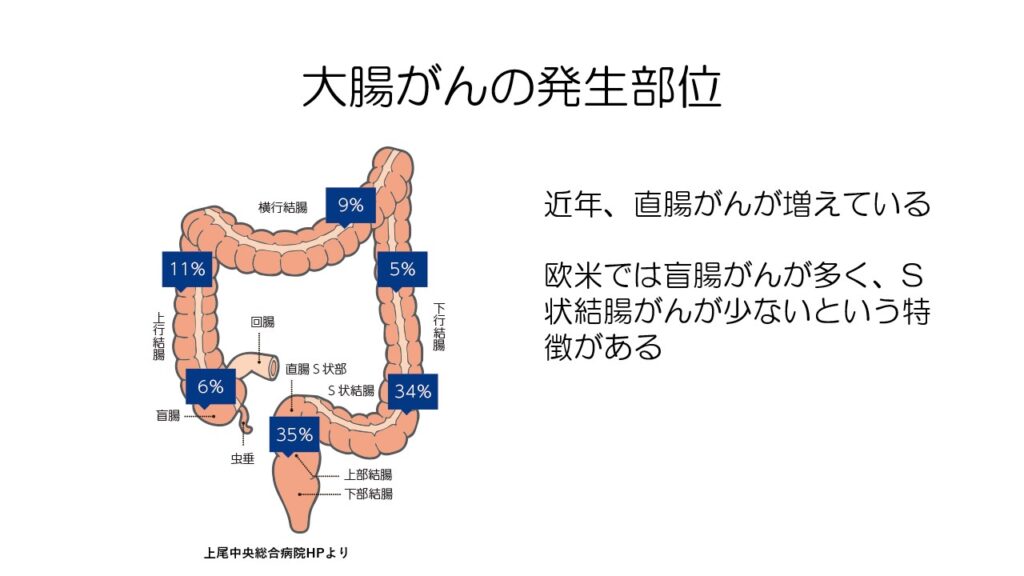

大腸がんは日本人S状結腸と直腸に最も多く見られ、この2か所に7割近く発生します。
欧米ではS状結腸がんは少なく、盲腸がんが多いという特徴があります。
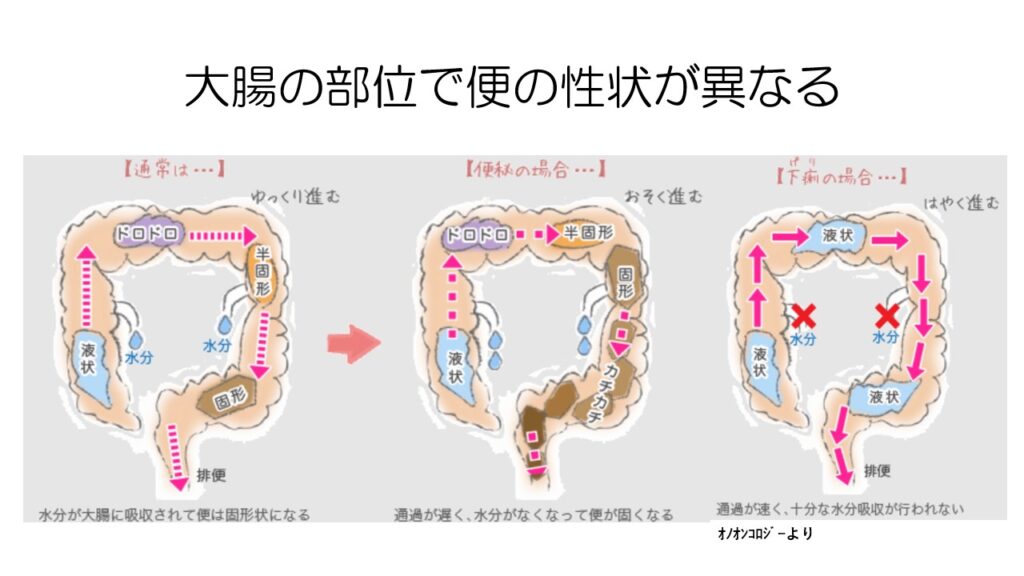

小腸から大腸に入ったすぐは、便は柔らかい液状で、大腸の中を進むにつれて水分が吸収され固形になっていきます。
便秘の場合は大腸の中にとどまっている時間が長く、水分が多く吸収され硬い便になります。
逆に下痢の場合は、水分が吸収されるよりも速く進むので、液状のままで排出されます。
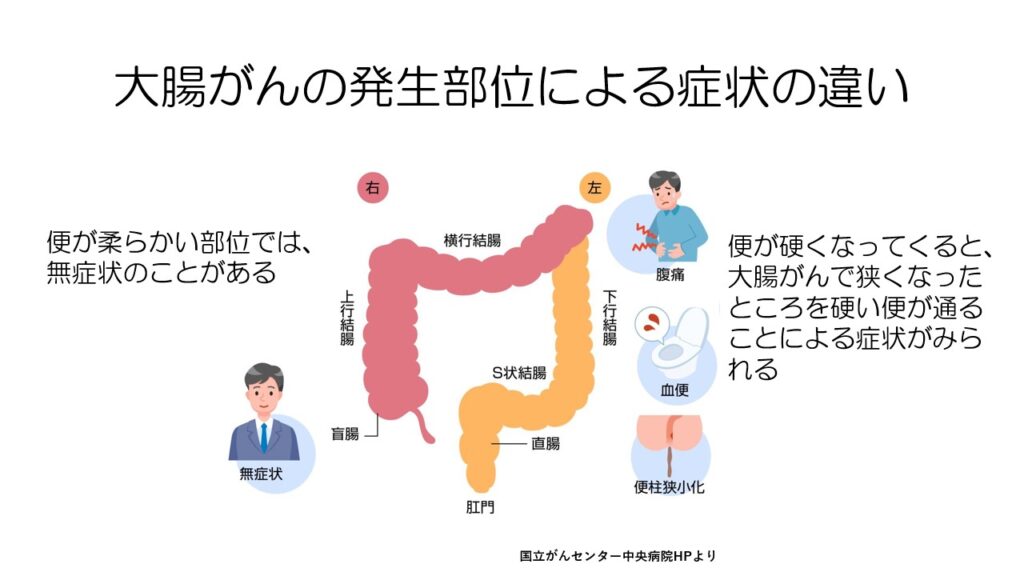

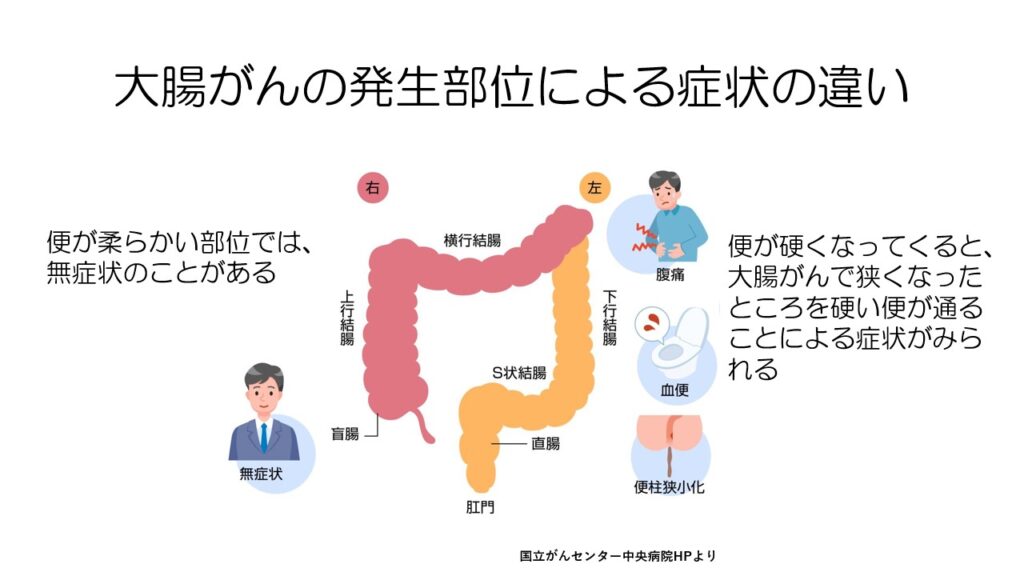
大腸がんは発生部位により症状が異なります。
大腸の左側である下行結腸から直腸では便が硬くなり、大腸がんで狭くなった部位を硬い便が通ることで、腹痛や血便などの症状が見られることがあります。
逆に大腸の右側である盲腸から横行結腸までの部位では、便が柔らかい状態なので、がんが進行しても無症状のことがあります。
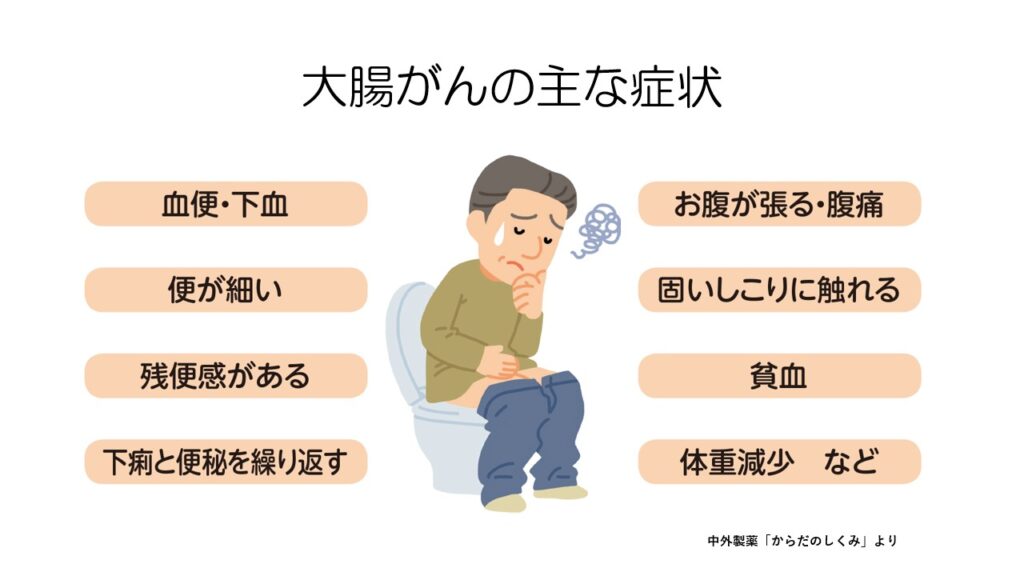

大腸がんの症状は血便や腹痛以外にも多くの症状が見られます。
これらの症状は早期がんではほぼ見られず、進行がんで見られます。
大腸がんのリスク


大腸がんのリスクを上げる因子に飲酒、喫煙、肥満、加工肉などがあります。
喫煙者は大腸がんのリスクが1.4倍に、お酒をよく飲む男性はリスクが2.1倍となります。
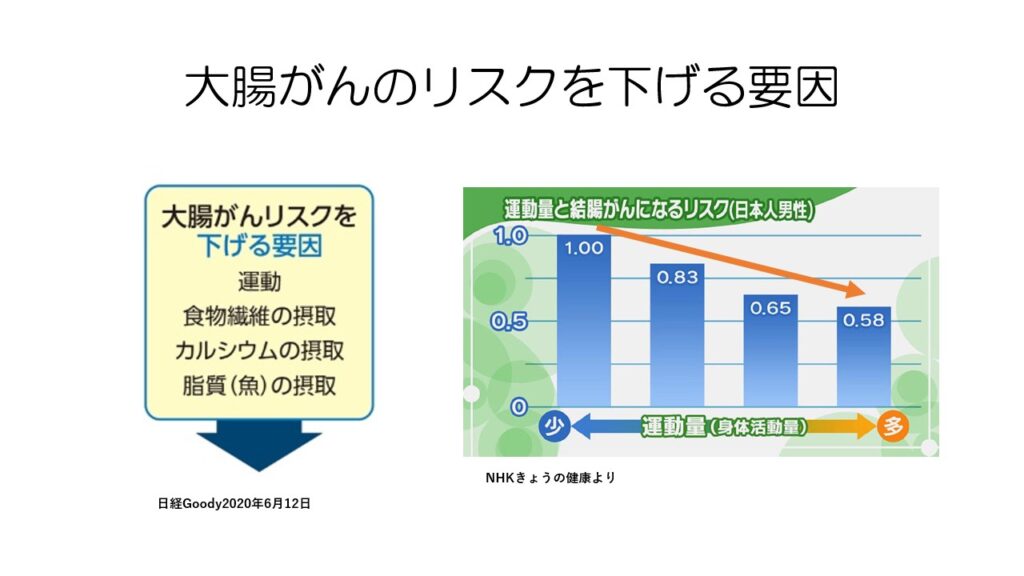

大腸がんのリスクを下げる因子で最も影響が大きいのが運動です。
大腸がんの中でも、「男性」の「結腸がん」で最もリスクが低下します。
大腸がん検診


大腸がんを調べる方法として、最も簡便でよく行われているのが大腸がん検診です。
便に血液が混じっていないかを調べる便潜血検査を行います。
40歳以上で1年に1回検診があります。
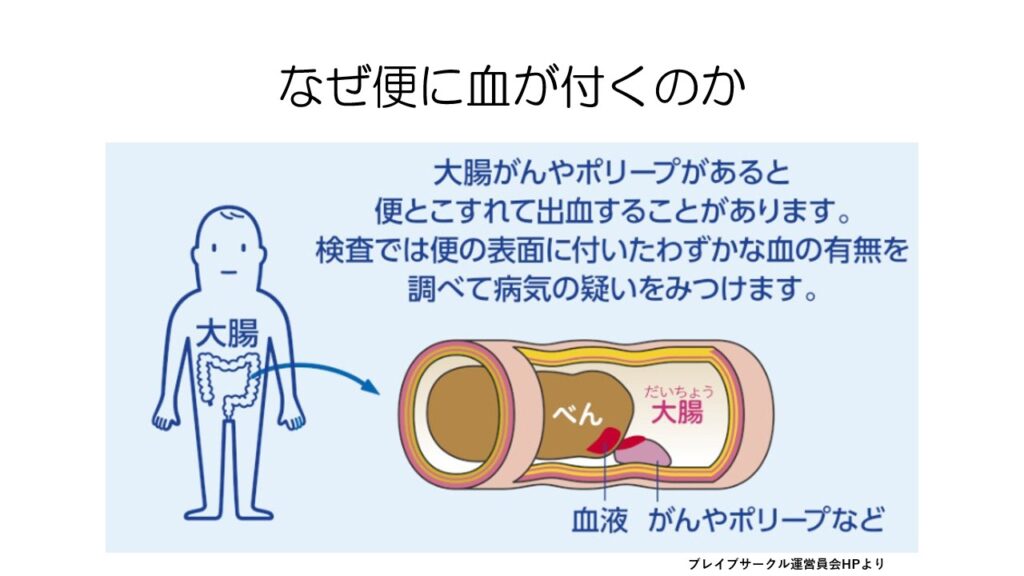

大腸がんやポリープは、便と擦れて出血することがあります。
そのわずかな血液を調べるのが便潜血検査です。
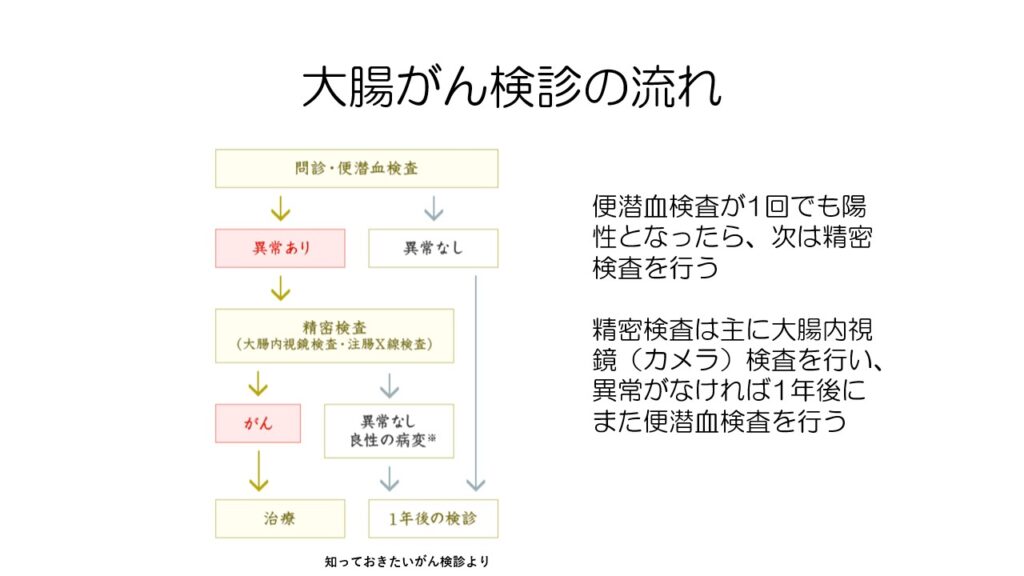

大腸がん検診で陽性と判定されたら、精密検査を受けるよう案内がきます。
精密検査は昔はバリウムの注腸検査も行っていましたが、現在は大腸内視検(大腸カメラ)検査が行われます。
もしそれで異常がなければ1年後にまた便潜血検査を行います。
大腸がんのステージと治療法

大腸がんのステージ0~2は、がんが大腸の壁に浸潤している深さで決まります。
リンパ節に転移があればがんの深さにかかわらずステージ3で、遠隔転移があればステージ4となります。
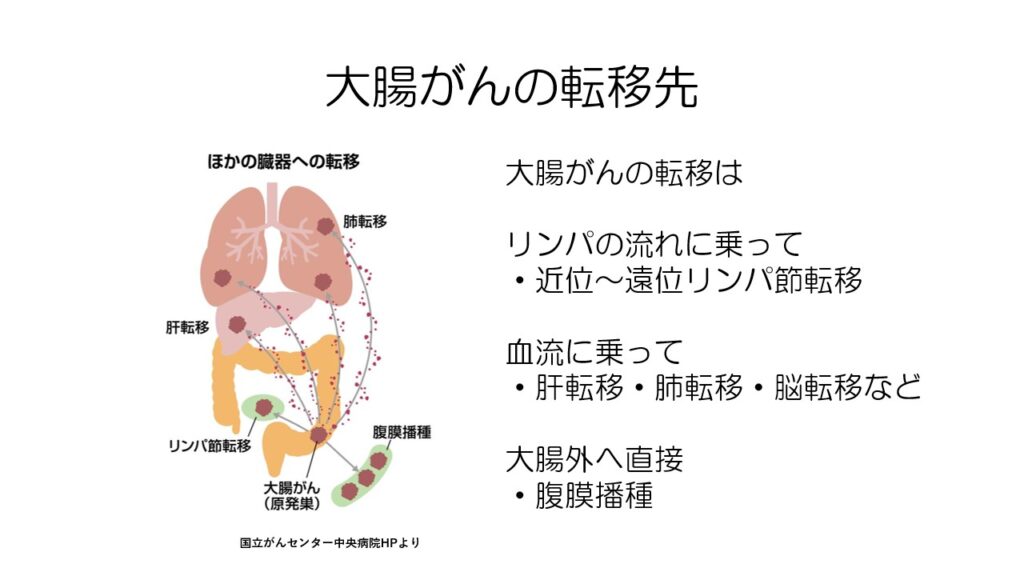

大腸がんの転移の仕方に3通りあります。
がん細胞がリンパの流れに乗って起こるリンパ節転移、血流に乗って起こる肝臓や肺への転移、大腸の壁を突き破って腹腔内に転移する腹膜播種があります。
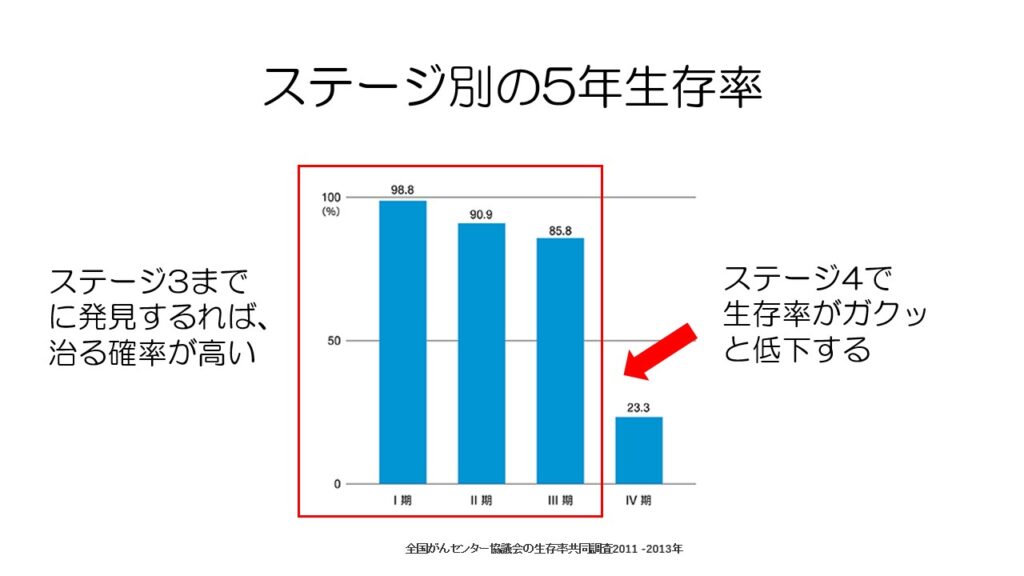

少し古いデータですが、大腸がんのステージ別の5年生存率です。
ステージ3までは高い生存率を保っており、つまり治る確率が高いです。
しかし、ステージ4になると生存率が極端に低下します。
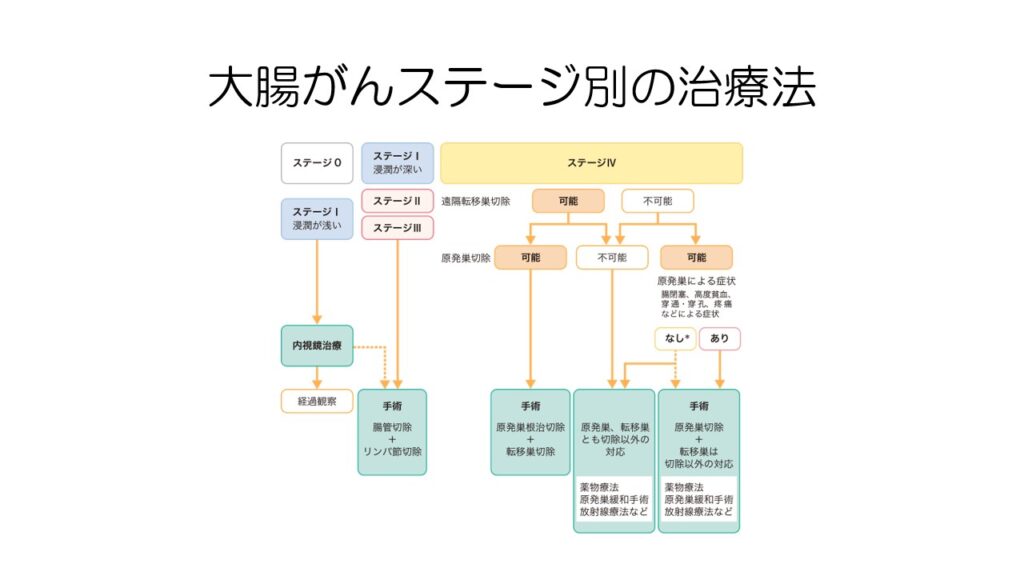

ステージ別の治療ガイドラインです。
内視鏡的切除も含め、大腸がんでは主に手術が行われます。
ステージ4でも、原発巣と遠隔転移巣の両方が切除可能であれば手術を行います。
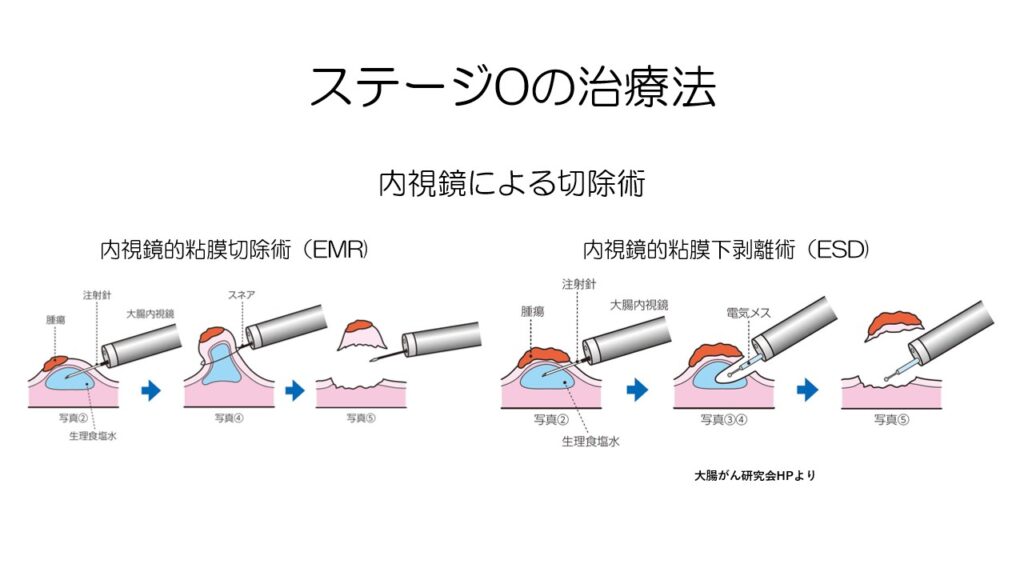

ステージ0の大腸がんは粘膜の表面に浅く存在するため、内視鏡で見ながら切除します。
内視鏡による切除には2通りの方法があります。
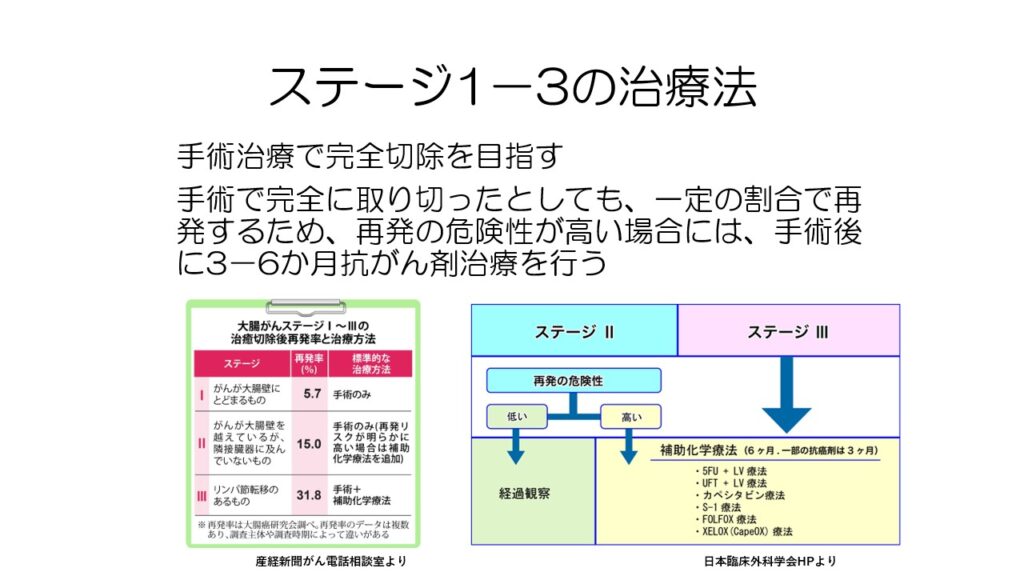

ステージ1~3は手術で完全切除を目指します。
ただ、見た目にすべて取り切っても再発することがあります。
ステージ2では15%、ステージ3だと1/3の確率で再発するため、術後に抗がん剤治療が行われます。
術後の抗がん剤については後ほど説明します。
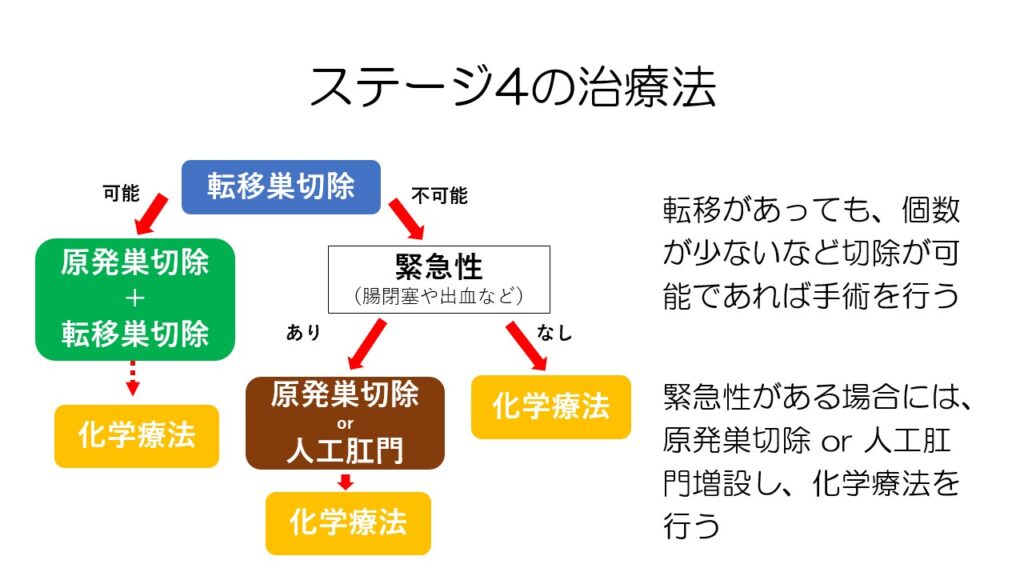

大腸がんは他のがんと異なり、ステージ4でも手術が行われます。
肺転移や肝転移があっても手術ですべて取り切れそうな場合には、原発巣も含めて完全切除を目指します。
腸閉塞や命にかかわるような出血が見られる場合には、症状を回避するための手術を行い、その後化学療法となります。
大腸がんの手術法
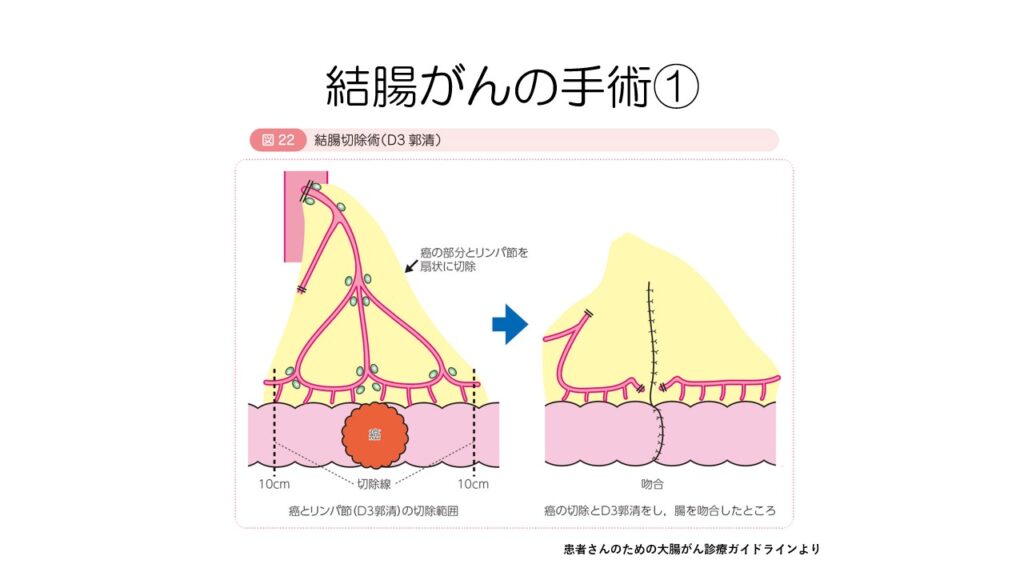

手術は、がんから十分距離を離して大腸を切除し、転移する可能性のあるリンパ節も切除します。
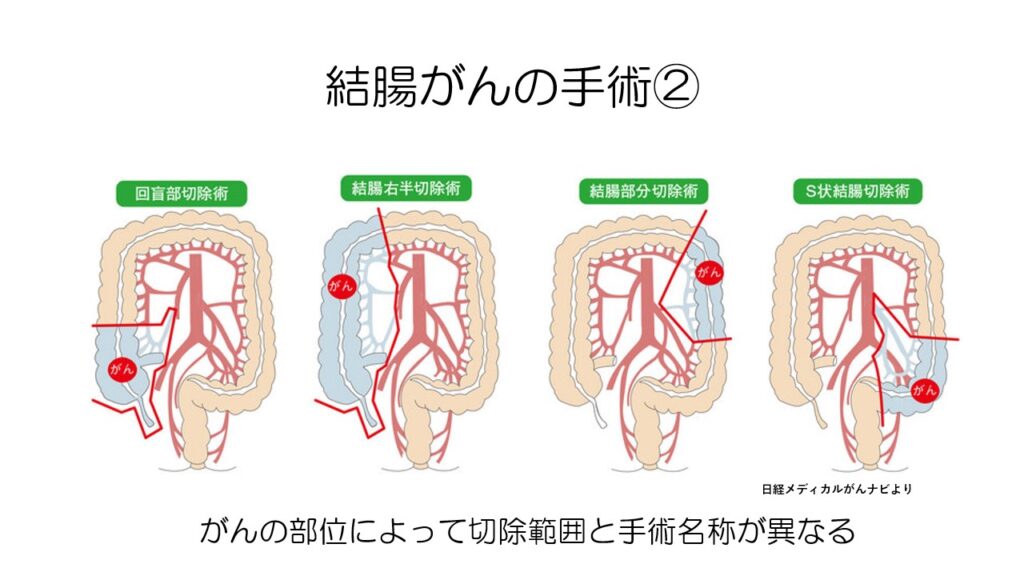

がんの発生部位によって手術の名称が異なります。
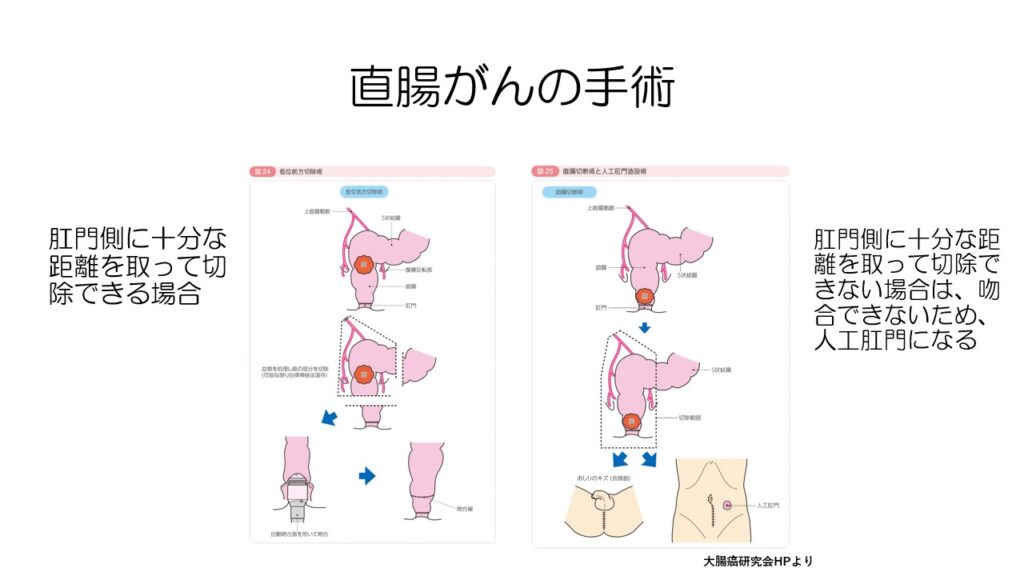

直腸がんの場合は、手術方法が少し異なります。
左の図のように肛門側に十分な距離を取って切除できる場合には吻合しますが、肛門に近い場合には吻合ができないため、肛門を切除し人工肛門を作成します。
大腸がんの薬物治療
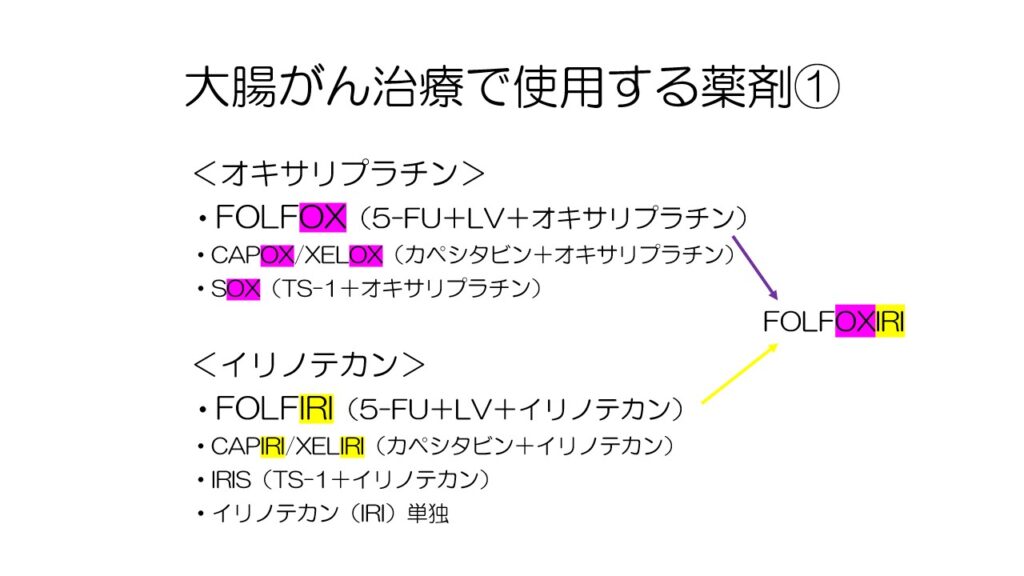

オキサリプラチンとイリノテカンが2大キードラッグです。
それぞれいくつかのレジメンがあり、5-FUとオキサリプラチンを合わせたFOLFOX、5-FUとイリノテカンを合わせたFOLFIRIがよく使われます。
5-FUとオキサリプラチン、イリノテカンを合わせたFOLFOXIRIという治療法もあります。


オキサリプラチンとイリノテカン以外の抗がん剤は、内服の抗がん剤がほとんどです。
ロンサーフ、スチバーガは三次、四次治療で使用され、最近五次治療薬のフリュザクラが承認されました。


分子標的薬は主に抗がん剤と併用して用いられます。
出血などの心配がない場合には、血管新生阻害薬が用いられます。
後ほど出てきますが、一定の条件を満たした大腸がんでは化学療法と併用してEGFR阻害薬が使用されます。


こちらの分子標的薬は主に遺伝子パネル検査で調べる遺伝子に異常があった場合に使用されます。
二次治療、三次治療以降で使用されます。


こちらも後ほど出てきますが、マイクロサテライト不安定が見られた場合には、免疫チェックポイント阻害薬を使用します。
薬物療法の副作用


大腸がん治療で使われる薬剤の副作用についてお話しします。
ほとんどの抗がん剤に共通する副作用はこちらで、多くに人がイメージする副作用かもしれません。


共通した副作用以外で、各抗がん剤に特徴的な副作用というのがあります。
キードラッグであるオキサリププラチンに特徴的な副作用はしびれと痛みです。
寒冷刺激で悪化するため、冷たい物を触ったり飲み込んだりすると痛みが強くなります。
イリノテカンの特徴的な副作用は下痢です。
UGT1A1という遺伝子に異常があると、イリノテカンの副作用が強く出ることが分かっており、大腸がんの治療前に必ず調べます。
カペシタビンやTS-1は涙の通り道である涙道が詰まって涙が止まらなくなるという副作用があります。


血管新生阻害薬であるアバスチンなどには、高血圧やタンパク尿など他の薬剤にはあまり見られない副作用があります。
また、消化管穿孔という重篤な副作用が起こる可能性があります。


HER2阻害薬のハーセプチン、パージェタ、フェスゴの副作用で注意するのは心機能低下です。
ビラフトビ、メクトビは手足の障害や眼の障害をはじめ、皮膚がんという珍しい副作用があります。


免疫チェックポイント阻害薬は、すべての臓器で様々な副作用が出る可能性があり、副作用の管理が難しい薬剤です。
術前・術後の補助療法


ステージ2の一部やステージ3の場合は再発を予防するために手術後に抗がん剤治療を行います。
再発リスクが高い場合には、オキサリプラチンベースの強い抗がん剤治療を3-6か月行います。
再発リスクが低い場合や高齢者の場合には、内服の抗がん剤や比較的弱い点滴の抗がん剤が用いられます。
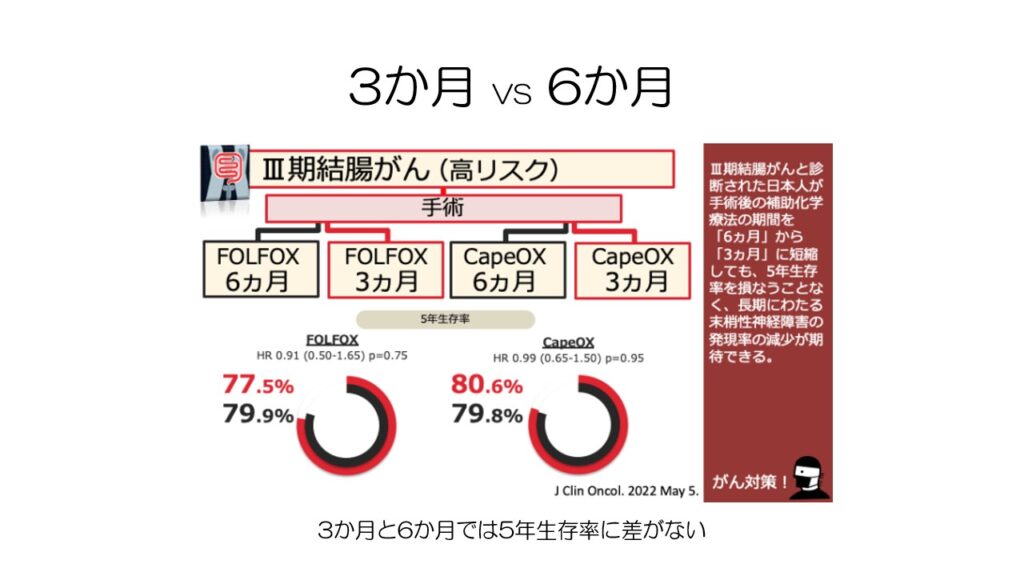

術後の抗がん剤治療は、3か月間行うのと6か月間行うのでは差はないので、3か月が基本です。
再発リスクが非常に高い症例では、6か月間行うこともあります。


日本では手術が第一選択で、手術前に抗がん剤治療を行うことはほとんどありませんでした。
海外では直腸がんに限ってですが、手術前に化学放射線療法を行うことが多く、局所再発を減らしたり手術を回避できたりすることがあります。
ちなみに、結腸がんでは放射線療法が難しく、化学放射線療法は行いません。
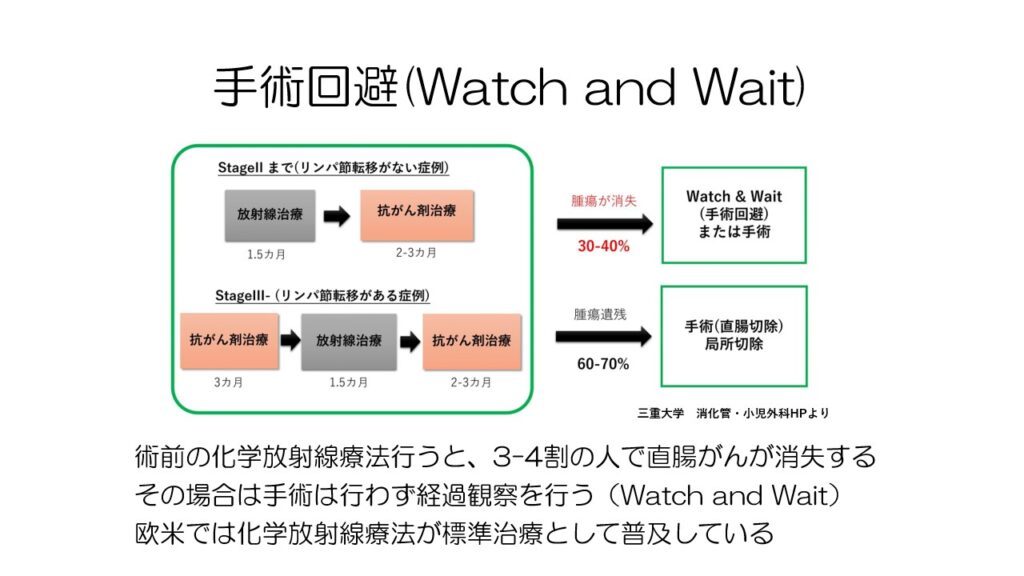

直腸がんで術前化学放射線治療を行うと、3-4割の症例でがんが消失します。
その場合はWatch and Waitと言って、慎重な経過観察をしながら手術を行わず様子を見る方法がとられます。
欧米では、ステージ2-3の直腸がんで化学放射線治療後のWatch and Waitが標準治療の一つとなっています。
日本でも最近は行う施設が増えてきました。
坂本龍一さんも海外で直腸がんに対して化学放射線療法を行ったようですが、残念ながらがんが残ってしまい、日本で手術を行いました。
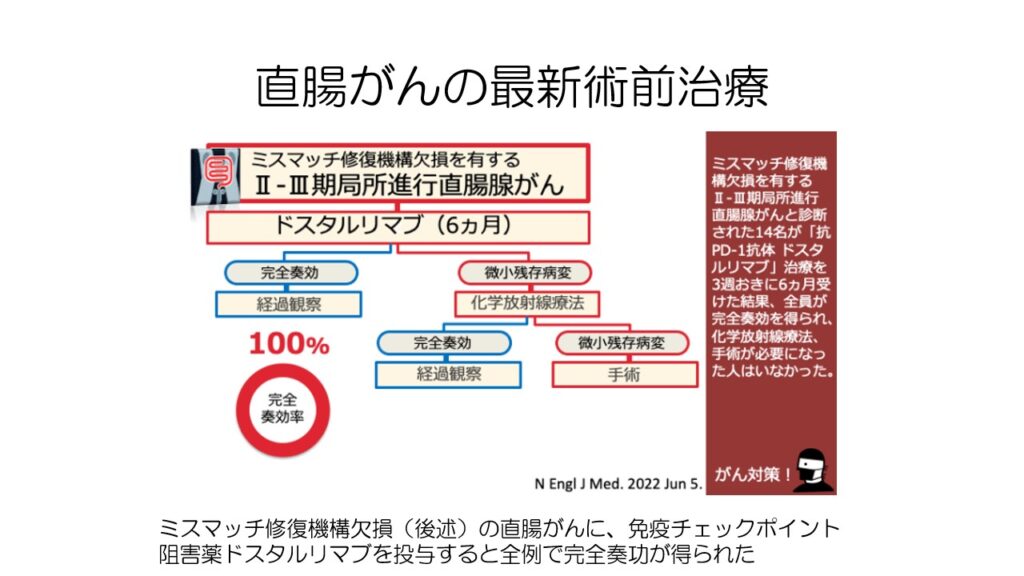

ミスマッチ修復機構欠損のある直腸がんに対して免疫チェックポイント阻害薬ドスタルリマブを投与すると、なんと100%全例で完全奏功が得られるという衝撃の発表が数年前にありました。
ミスマッチ修復機構欠損のある直腸がんでは、今後は抗がん剤も放射線治療も手術も不要となる可能性があります。
日本では2023年に臨床試験が始まったばかりなので、承認されるとしてもだいぶ先になります。
ミスマッチ修復欠損については後述します。
ステージ4の一次治療


大腸がんで生検や手術を行った際に、遺伝子異常に関連する項目を調べます。
これらはステージ4で化学療法を行う際の治療方針にかかわります。
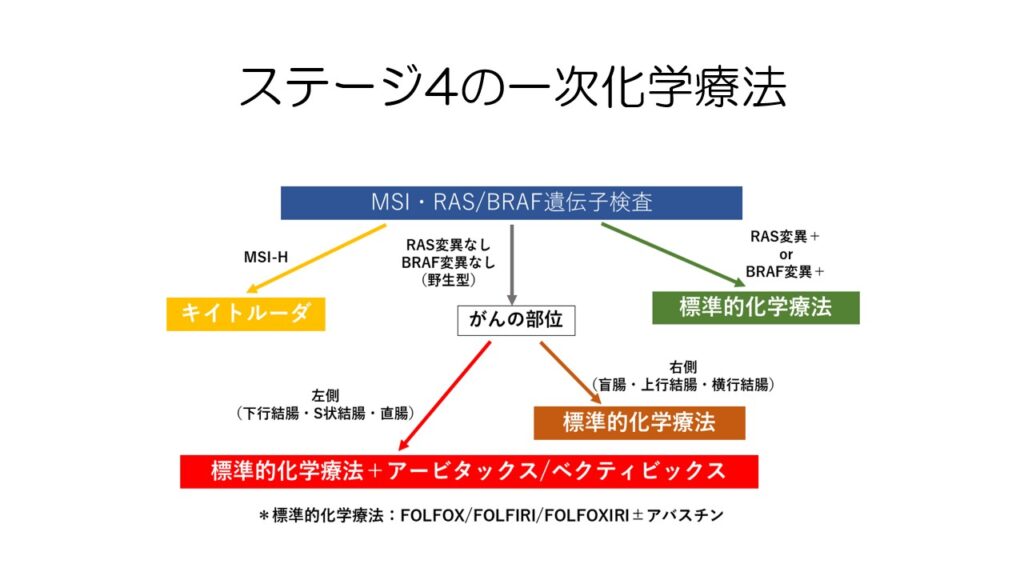

こちらは、ステージ4で抗がん剤治療となった場合のフローです。
MSI(マイクロサテライト不安定性)検査で、MSI-H(マイクロサテライト不安定)と診断されたら、抗がん剤治療ではなく免疫チェックポイント阻害薬であるキイトルーダを使用します。
RAS変異やBRAF変異がない場合には、真ん中の矢印に進みます。
左側(下行結腸から直腸)の大腸がんの場合には、EGFR阻害薬であるアービタックスやベクティビックスを抗がん剤治療と併用します。
右側結腸の場合やRAS変異やBRAF変異が見られる場合には、EGFR阻害薬が効かないので、抗がん剤治療のみとなります。
この辺りは銀座みやこクリニックのアメーバブログで細かく解説していますので、ぜひそちらもご覧ください。
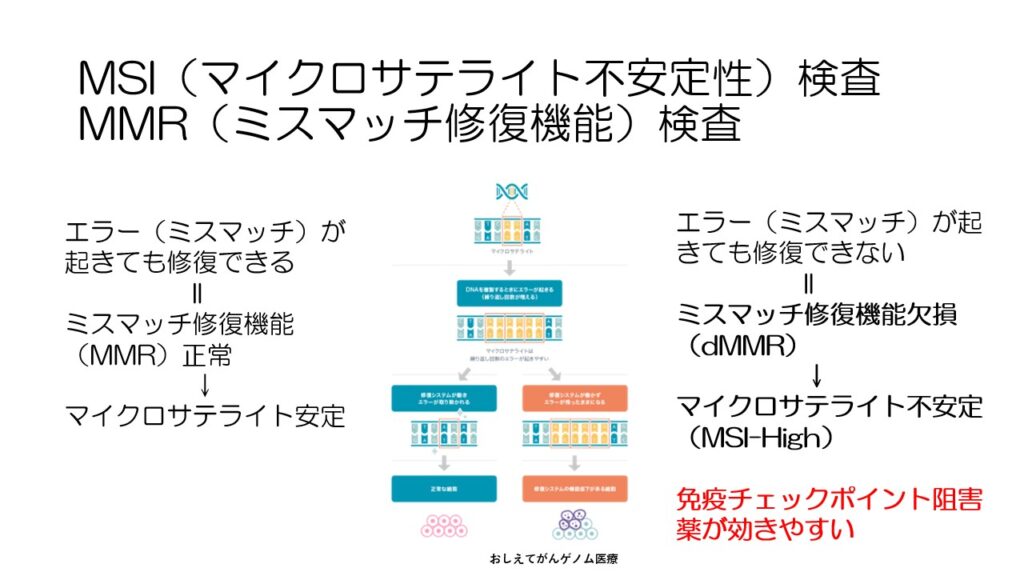

MSI検査について。遺伝子のエラーが起こった際に、修復する機能が壊れている状態を、dMMRミスマッチ修復欠損やMSI-Hマイクロサテライト不安定と言います。
壊れている状態の時は免疫チェックポイント阻害薬が効きやすいです。
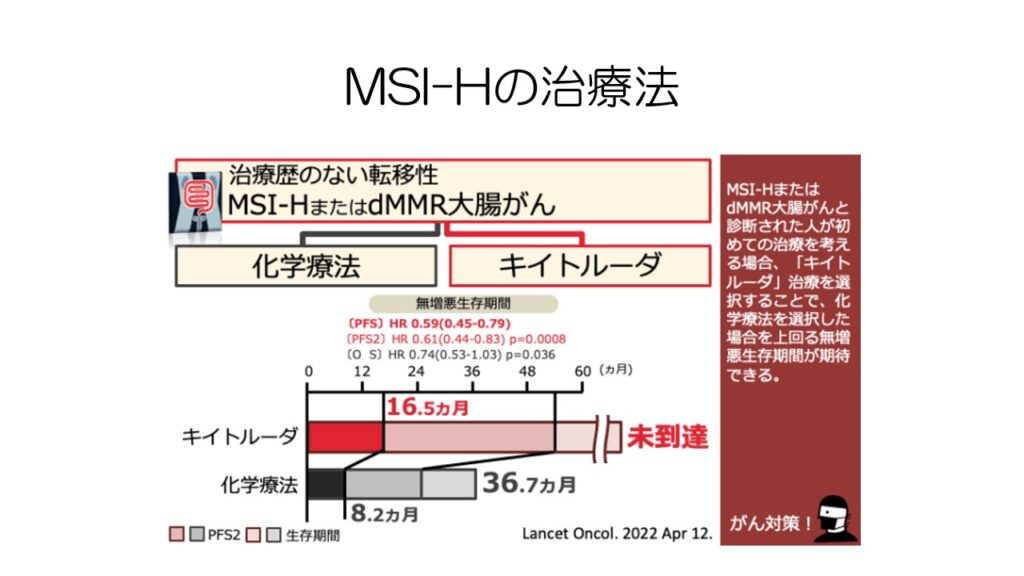

がんの治療=抗がん剤と思われがちですが、MSI-H(マイクロサテライト不安定)の場合には、免疫チェックポイント阻害薬キイトルーダが抗がん剤よりも高い治療効果を発揮します。
先ほどのミスマッチ修復欠損の直腸がんも免疫チェックポイント阻害薬がよく効いていましたね。
ステージ4の二次治療以降
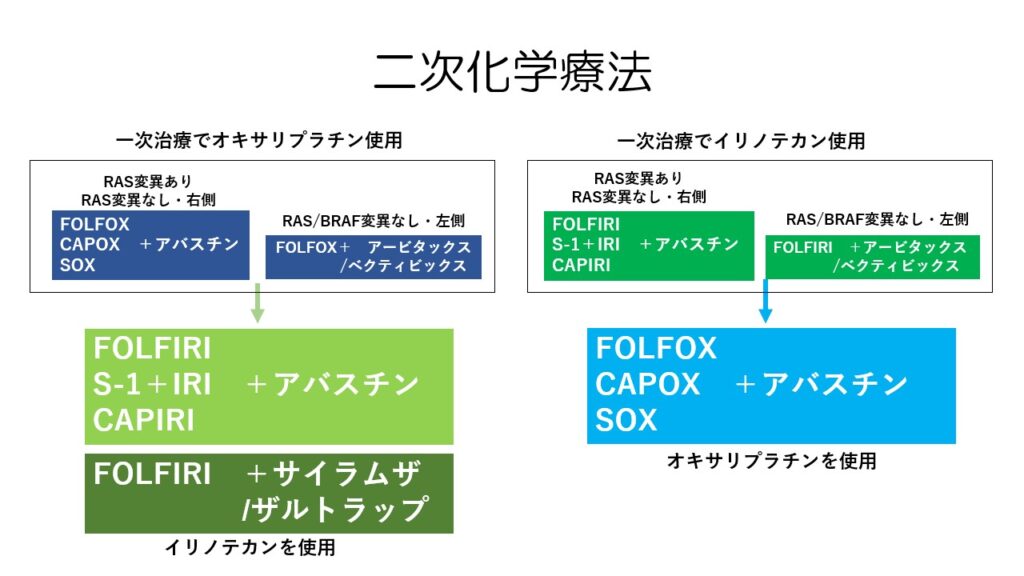

標準的な抗がん剤治療では、一次治療でオキサリプラチンを使用した場合、二次治療ではイリノテカンを使用します。
逆に一次治療でイリノテカンを使用した場合には、二次治療でオキサリプラチンを使用します。
この2大キードラッグを使い切るのが大腸がん治療のポイントです。
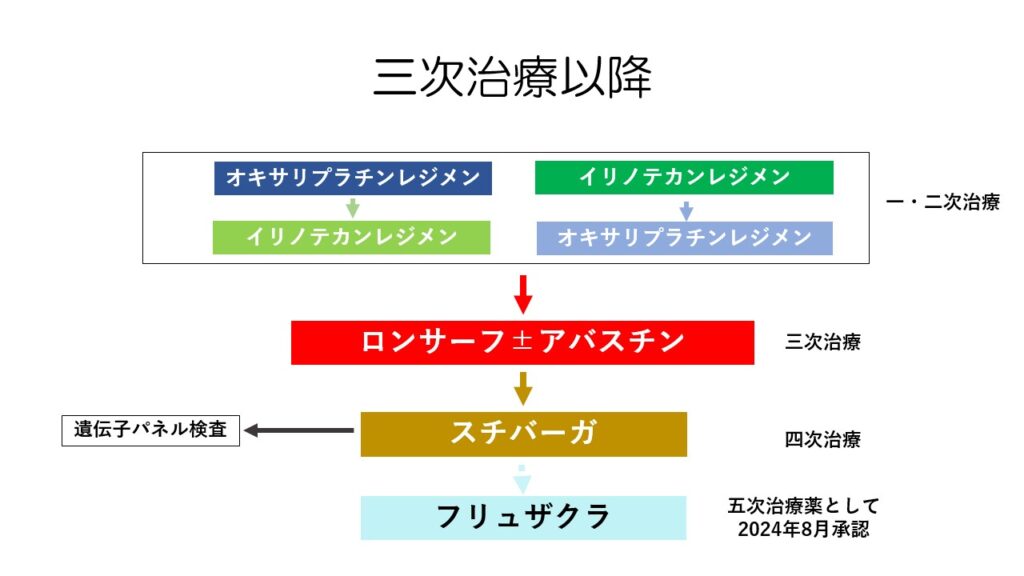

三次治療はロンサーフ、四次治療はスチバーガ使われます。
五次治療薬として、2024年8月にフリュザクラが承認されました。
四次治療まで行くと遺伝子パネル検査を保険で受けることができます。
遺伝子パネル検査の結果で、次のスライドで紹介するような治療の幅が広がります。
大腸がんの個別化医療
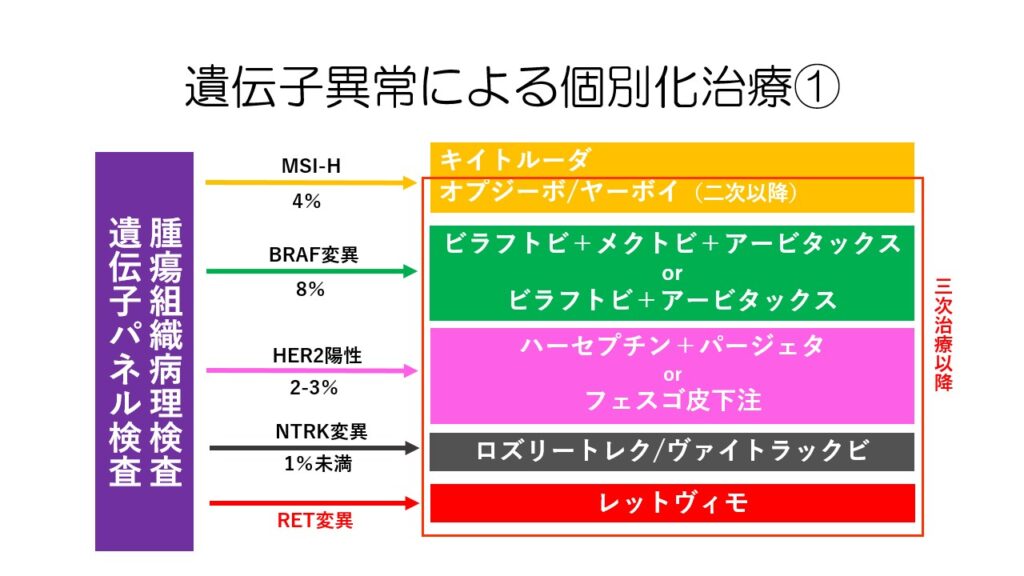

病理検査や遺伝子パネル検査の結果で遺伝子に関する異常が見られた場合には、三次治療以降で免疫チェックポイント阻害薬や分子標的薬を使用することができます。
異常が見つかる確率は高くないですが、もし異常があればこれらの薬剤を使用することができます。
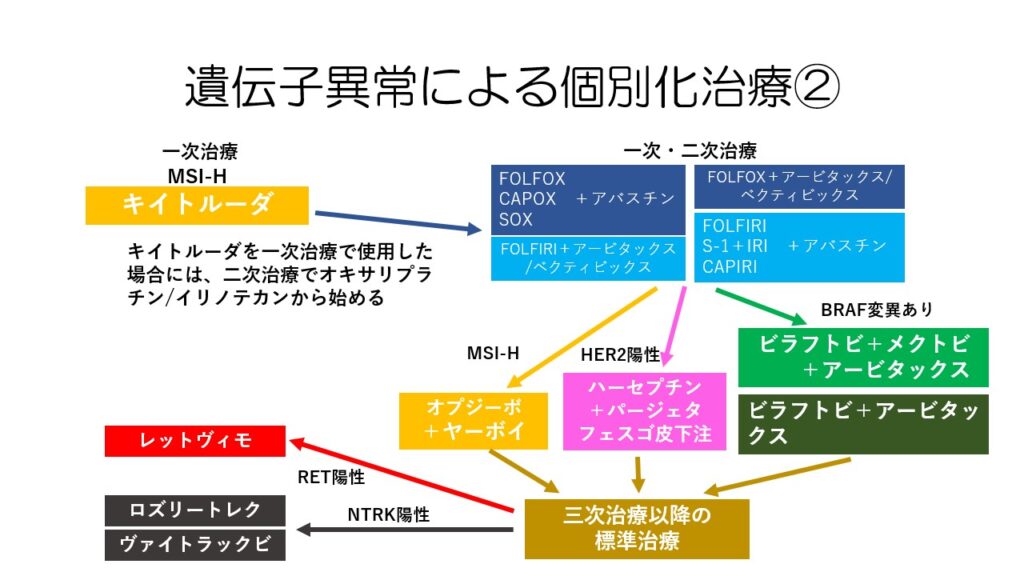

個別化治療についてのフローをまとめた図です。
この辺りも詳しく知りたい方は、銀座みやこクリニックのアメーバブログをご覧ください。
期待される大腸がん治療
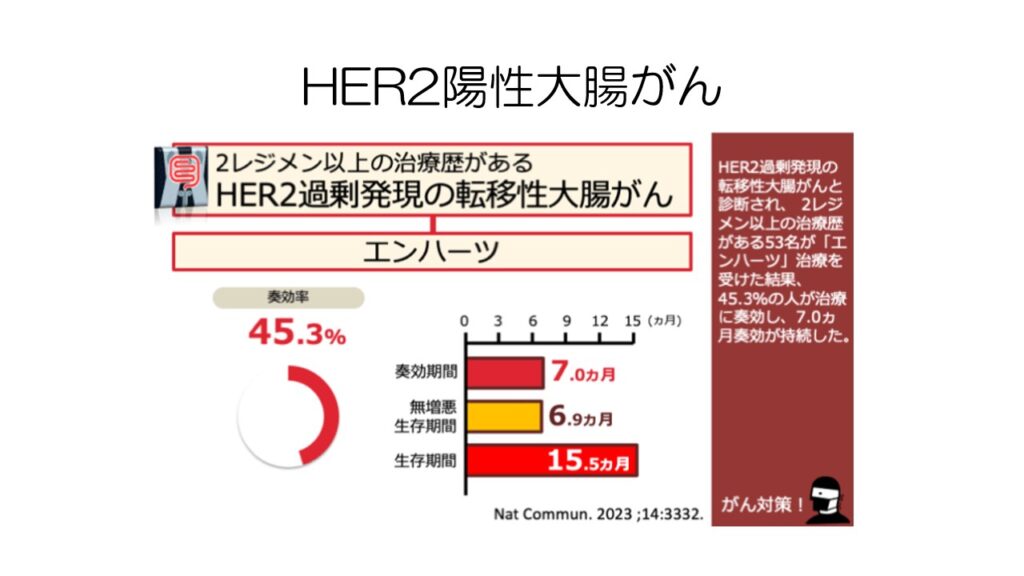

HER2陽性大腸がんの場合は、三次治療以降にハーセプチン+パージェタもしくはフェスゴが使われます。
さらに奏効率の高いエンハーツも今後承認されると思います。
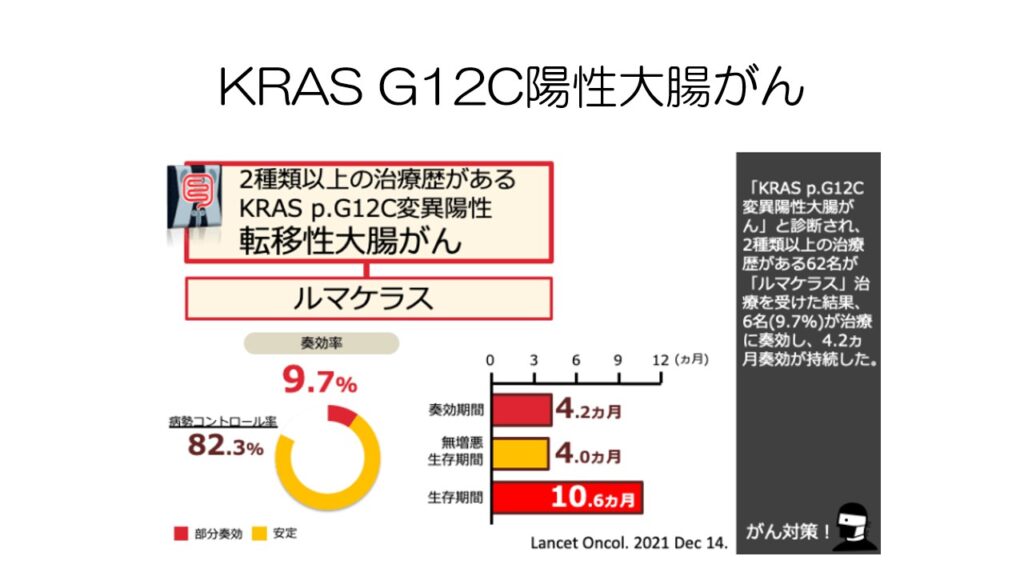

肺がんのKRAS G12C変異で承認されているルマケラスが、大腸がんでも有効性が示されています。
こちらも将来に承認される可能性があります。
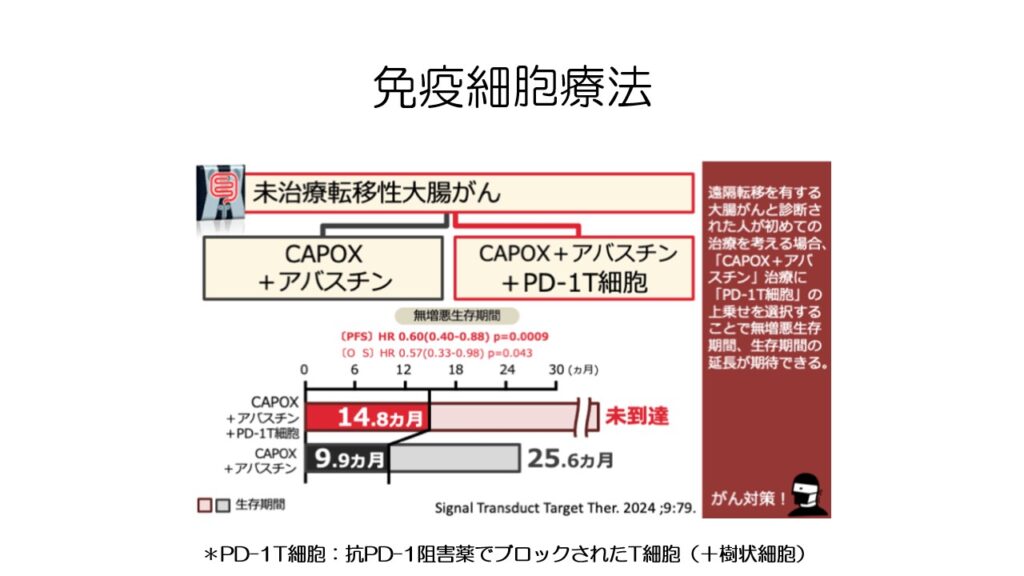

全く新しいタイプの治療法が開発されています。
キラーT細胞を免疫チェックポイント阻害薬とともに培養し、免疫チェックポイント阻害薬の効果を持ったT細胞が中国で作成されました。
こちらは従来の化学療法と併用し無増悪生存期間と生存期間が延長したという研究です。
免疫チェックポイント阻害薬を点滴するよりも副作用が軽く、安全性が高い治療の可能性があります。
今年2024年に発表されたばかりなので今後の研究に期待です。
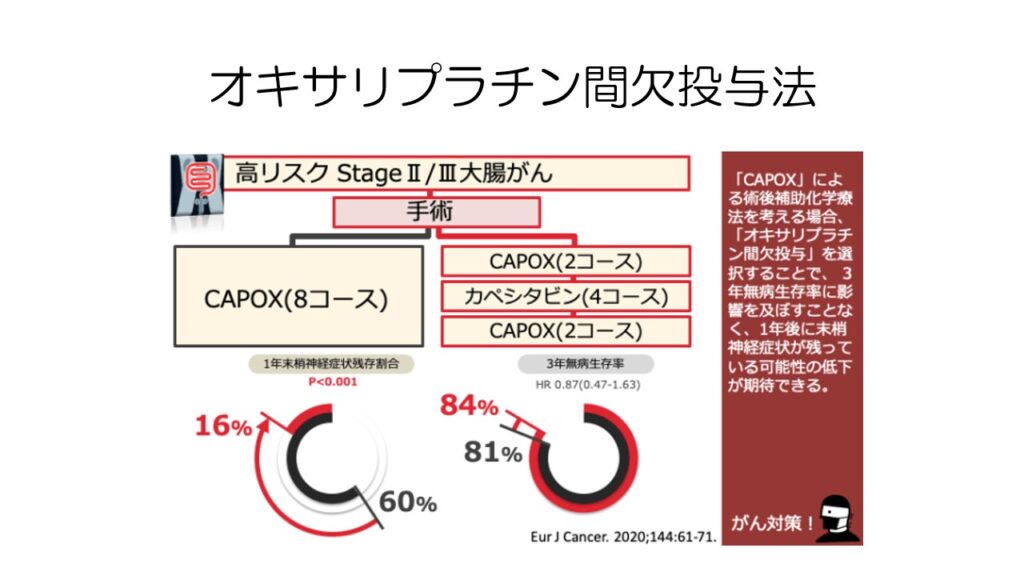

カペシタビン+オキサリプラチンを投与する術後のCAPOX療法で、副作用を軽減させるために途中でオキサリプラチンを抜く間欠投与法の研究があります。
間欠投与でも無病生存期間は変わらず、末梢神経障害の残存率が大幅に低下しました。
オキサリプラチンによる長期間の末梢神経障害を少しでも減らすために、このような治療法がもっと研究されて欲しいと思います。
高齢者大腸がんの治療の工夫
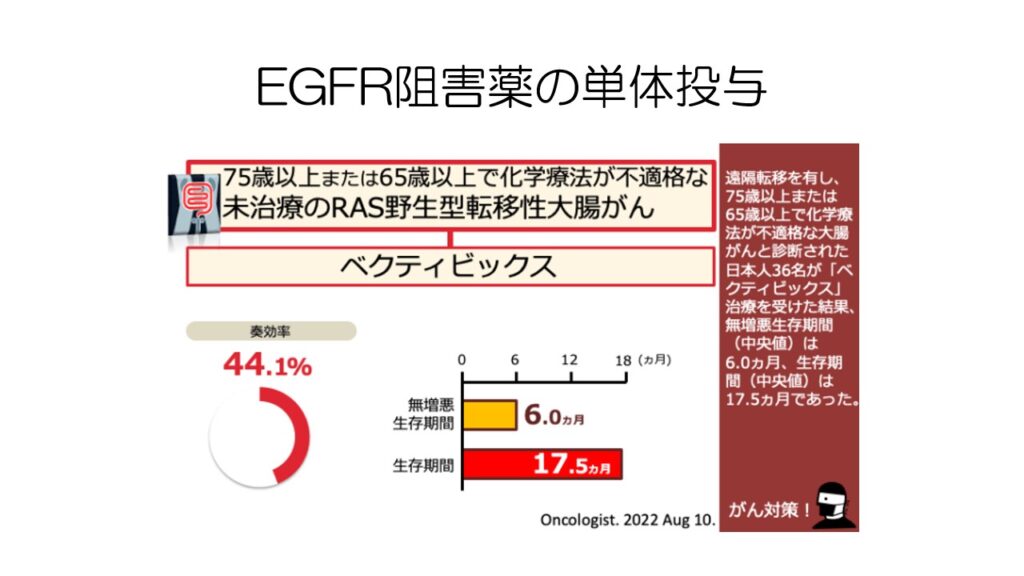

高齢などの理由で抗がん剤治療ができない左側大腸がんの患者さんに対して、分子標的薬のベクティビックスのみを投与した日本での臨床試験です。
分子標的薬のみでも高い奏効率と生存期間が得られるようです。
左側結腸がんで、RAS変異のない高齢者では、副作用の強い抗がん剤をせず、分子標的薬だけを投与するというのも選択肢として考えられます。


















コメント